��Ŀ����
����Ŀ�������������ʵ���һ�ҵ���������пɳ�������ͼʾ��ת���� 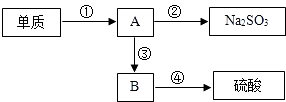
��1��ʵ�����У���������ɫ���壬��ȼ�����������ڳ��������ļ���ƿ��ȼ�գ�����Ư��������ɫ���棬��������A��
��2��A�ǹ�ҵ�ŷ�����һ����Ҫ�Ŀ�����Ⱦ�Ҳ�������γɵ�����֮һ��������ѧ����֪ʶ�ɽ�Aת����Na2SO3 �� ���ṩ���Լ�����Һ��
��3�������Ṥҵ�У���A��һ��������������е����ʷ�Ӧ�õ�B��B��ˮ��ϵõ����ᣮB��A�����Ԫ����ͬ��B����Ԫ������������Ԫ�ػ��ϼ���ͬ��д��Aת����B�Ļ�ѧ����ʽ�� �� ʵ���Ҳⶨ��B��ˮ���ʱ�¶����ߣ���Ӧ��Ϊ��Ӧ��ѡ����ȡ����ȡ�����
��4����������ת�������У����ڻ��Ϸ�Ӧ����������ţ���
��5�������չ�ҵ�ŷ���A 32�֣������Ͽ����������֣�
���𰸡�
��1����
��2����������
��3��2SO2+O2 ![]() 2SO3������
2SO3������
��4���٢ۢ�
��5��49
���������⣺��1���������ǻ�ɫ�Ĺ��壬����ƣ���2������������Ӧ���ɶ���������������������������Һ��Ӧ�����������ƺ�ˮ������������ƣ���3��������������������Ӧ������������������������ˮ��Ӧ�������ᣬB��ˮ��Ӧ�¶�����˵���÷�Ӧ�Ƿ��ȷ�Ӧ�����2SO2+O2 ![]() 2SO3 �� ���ȣ���4����Ӧ��������������Ӧ���ɶ����������ڻ��Ϸ�Ӧ����Ӧ���Ƕ����������������������������ƺ�ˮ�ķ�Ӧ�������ڻ�����Ӧ���ͣ���Ӧ���Ƕ�������������������������ķ�Ӧ�����ڻ��Ϸ�Ӧ����Ӧ��������������ˮ��������ķ�Ӧ�����ڻ��Ϸ�Ӧ������٢ۢܣ���5�����������������Ϊx 2SO2+O2
2SO3 �� ���ȣ���4����Ӧ��������������Ӧ���ɶ����������ڻ��Ϸ�Ӧ����Ӧ���Ƕ����������������������������ƺ�ˮ�ķ�Ӧ�������ڻ�����Ӧ���ͣ���Ӧ���Ƕ�������������������������ķ�Ӧ�����ڻ��Ϸ�Ӧ����Ӧ��������������ˮ��������ķ�Ӧ�����ڻ��Ϸ�Ӧ������٢ۢܣ���5�����������������Ϊx 2SO2+O2 ![]() 2SO3 �� SO3+H2O=H2SO4
2SO3 �� SO3+H2O=H2SO4
SO2���� | H2SO4 |
64 | 98 |
32t | x |
![]() x=49t
x=49t
���49��
�����㾫����������Ŀ����֪���������������Ļ�ѧ���ʺ���д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ�����֪ʶ���Եõ�����Ĵ𰸣���Ҫ���������Ļ�ѧ���ʣ����е����ʣ�֧��ȼ�գ�����������ע�⣺a����ƽ b������ c�����ţ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ��ijУѧϰС����̽������IJⶨ�����ݴ��������� ��������⡿
�������ʯ��ʯ����Ҫ�ɷ�ΪCaCO3����ϡ���ᷴӦ���ⶨ����CO2����������������������ݣ�
��ʵ����ơ�ͨ����������ʵ��ֱ�ⶨCO2�������������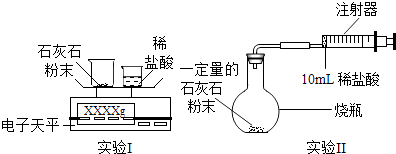
����������
��1����������ʵ���У���Ӧ�Ļ�ѧ����ʽ�� ��
��2��ʵ����У���С�ձ��е�����ϡ����ּ��μ��뵽���ձ��У������Ͻ��裬�ж�ʯ��ʯ��CaCO3��ȫ��Ӧ��ʵ�������� ��
��3��ʵ����У������Ӻ�װ�ã�������������ƣ���Ȼ��װ��ҩƷ�����10mlϡ�������������ƿ�У���ϡ�����ǻ�������ģ��������ɵĺ���� ��
��4������¼�봦���� ��֪ʵ��I��Ӧǰ��������[m�����ձ�+ʯ��ʯ��ĩ��+m��С�ձ�+ϡ���ᣩ]��Ҫ��������CO2�����������ٻ���Ҫ�������� ��
A.m��С�ձ���
B.m�����ձ���
C.m�����ձ�+��Ӧ��ʣ���
��5��ʵ����ʵ���¼���£�������������ͬ�¶ȡ���ͬѹǿ�����²ⶨ����
ʱ��/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
ע��������/ml | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
�ٸ�������ʵ����̺������ۺϷ�������������CO2�������ml�������� ��
�ڸ��������ʶ��������ͼ�л��Ƴ�0��10min����CO2�����ʱ��仯������ �� 
��6������˼�����ۡ� ��������������Ϊʵ��I���ŵ��� �� ʵ�����ŵ��� ��