题目内容
【题目】将一定量的乙醇(C2H6O)和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表。则下列说法正确的是
物质 | 乙醇 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 4.6 | 8.0 | 0 | 0 | 0 |
反应前质量/g | 0 | 0 | 5.4 | 4.4 | a |
A.表中a的值为2.6
B.X一定是该反应的催化剂
C.X可能含有氢元素
D.若起始时氧气的质量是10g,则无x生成
【答案】D
【解析】
A、由表中数据分析可知,反应前后,乙醇的质量减少了4.6g,故乙醇是反应物,参加反应的乙醇的质量为4.6g;同理可以确定氧气是反应物,参加反应的氧气的质量为8.0g;水是生成物,生成的水的质量为5.4g;生成二氧化碳的质量为4.4g;由质量守恒定律,X应是生成物,且生成的X的质量为4.6g+8.0g-5.4g-4.4g=2.8g,故表中a的值为为0g+2.8g=2.8g;故选项说法错误。
B、由A选项分析可知,X的质量增加,故一定不是该反应的催化剂,故选项说法错误。
C、根据反应前后元素质量不变,反应物乙醇中含氢元素的质量为![]() ,生成物水中含氢元素的质量为
,生成物水中含氢元素的质量为![]() ,氢元素的质量相等,故X中不含氢元素;故选项说法错误。
,氢元素的质量相等,故X中不含氢元素;故选项说法错误。
D、乙醇完全燃烧的化学方程式为:C2H5OH+3O2![]() 2CO2+3H2O根据乙醇燃烧的方程式可知,4.6克乙醇能与9.6克的氧气恰好完全反应,生成了二氧化碳和水,因此若起始时氧气的质量是10g,则无X生成;故选项说法正确。
2CO2+3H2O根据乙醇燃烧的方程式可知,4.6克乙醇能与9.6克的氧气恰好完全反应,生成了二氧化碳和水,因此若起始时氧气的质量是10g,则无X生成;故选项说法正确。
故选:D。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某学习小组在“利用燃碳法测定空气中氧气的体积分数”的实验时(如图装置),发现一个现象:氢氧化钠溶液吸收生成的二氧化碳后,进入集气瓶中氢氧化钠溶液的体积分数仍然小于1/5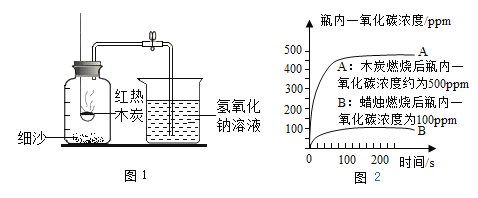 。
。
(1)木炭充分完全燃烧反应的化学方程式为_____。
(提出问题)
是什么原因导致测量的结果不准确呢?
甲同学:可能是木炭取用的量过少;
乙同学:可能是木炭燃烧没有消耗完集气瓶中的氧气;
丙同学:可能是木炭在密闭容器中燃烧生成了一氧化碳。
小组同学发现实验结束后,燃烧匙中还有残留的黑色固体,都认为甲同学的猜想不合理。
(查阅资料)
一氧化碳不与氢氧化钠溶液反应;木炭、棉花和蜡烛在密闭容器内燃烧停止后,残留氧气的体积分数高达14.0%、8.0%和16.0%。
(实验探究)
(2)乙同学根据图1装置设计了如下实验,请你填写下表。
实验步骤 | 实验现象 | 实验结论 |
1.将足量木炭点燃,迅速插入集气瓶中; 2.待冷却后,将燃着的_____(填“棉花”或“蜡烛”)再伸入该集气瓶中。 | _____ | 木炭燃烧_____(填“有”或“没有”)消耗完集气瓶中的氧气。 |
(交流反思)
(3)乙同学选择可燃物(“棉花”或“蜡烛”)的依据是_____。
(4)丙同学使用了CO浓度传感器测木炭、蜡烛分别在密闭集气瓶里燃烧停止后,瓶内CO的浓度变化,曲线如图2。根据此曲线图分析用上述装置不能准确测出氧气体积分数的原因_____。
(拓展提升)
通过研究性小组的探究,请你谈谈对物质燃烧的认识(两点):①_____;②_____。