题目内容
13g锌和87.4g一定浓度的稀硫酸恰好完全反应.求:
(1)生成氢气的质量;
(2)反应后所得溶液中溶质的质量分数.
(1)生成氢气的质量;
(2)反应后所得溶液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:锌和稀硫酸反应生成硫酸锌和氢气,根据锌的质量可以计算生成氢气、硫酸锌的质量,从而求出反应后所得溶液中溶质的质量分数.
解答:解:设生成氢气的质量为x,生成硫酸锌的质量为y,
Zn+H2SO4═ZnSO4+H2↑,
65 161 2
13g y x
=
y=32.2g
=
x=0.4g
(1)生成氢气的质量为0.4g
(2)反应后所得溶液中溶质的质量分数为:
×100%=32.2%
答案:
(1)生成氢气的质量为0.4g
(2)反应后所得溶液中溶质的质量分数为32.2%
Zn+H2SO4═ZnSO4+H2↑,
65 161 2
13g y x
| 65 |
| 13g |
| 161 |
| y |
y=32.2g
| 65 |
| 2 |
| 13g |
| x |
x=0.4g
(1)生成氢气的质量为0.4g
(2)反应后所得溶液中溶质的质量分数为:
| 32.2g |
| 13g+87.4g-0.4g |
答案:
(1)生成氢气的质量为0.4g
(2)反应后所得溶液中溶质的质量分数为32.2%
点评:本题主要考查学生运用化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目

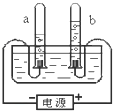 如图所示的是电解水实验装置.通电一段时间后,在A、B两个试管中分别收集到气体a和气体b.请回答:
如图所示的是电解水实验装置.通电一段时间后,在A、B两个试管中分别收集到气体a和气体b.请回答: