题目内容
【题目】科学小组的同学对模拟湿法炼铜实验中得到的铁、铜固体混合物进行含量测定,称取10克固体混合物置于烧杯中,滴加一定质量分数的稀硫酸溶液,记录并绘制了如图所示的曲线. 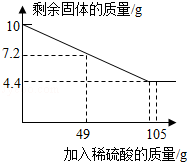
①10克固体混合物中铜的质量为g.
②所用稀硫酸溶液溶质的质量分数是多少?(写出计算过程).
【答案】解:①根据图示数据可知最后加入硫酸后固体质量不再减少,说明剩余的物质都是铜,10克固体混合物中铜的质量为4.4g;②根据图中数据可知,加入49g稀硫酸时消耗铁的质量是10g﹣7.2g=2.8g,设49g稀硫酸中溶质的质量为x,
Fe+ | H2SO4═FeSO4+H2↑ |
56 | 98 |
2.8g | x |
?? ![]()
x=4.9g
所用稀硫酸溶液溶质的质量分数是: ![]() =10%;
=10%;
答案:①4.4g;②所用稀硫酸溶液溶质的质量分数是10%.
【解析】①根据图示数据可知最后加入硫酸后固体质量不再减少,说明剩余的物质都是铜,再进行计算;②根据铁的质量结合化学方程式计算出消耗硫酸的质量,根据溶质质量分数的公式解答即可
【考点精析】解答此题的关键在于理解根据化学反应方程式的计算的相关知识,掌握各物质间质量比=系数×相对分子质量之比.

练习册系列答案
相关题目