题目内容
【题目】测定石灰石中碳酸钙的含量,设计如图所示:
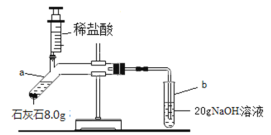
取8g石灰石样品,置于a中,并用20g氢氧化钠溶液吸收生成的气体。注入足量稀盐酸,充分反应,化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;当装置中不再产生气泡后,b试管中溶液为22.2g。
求:①根据以上实验数据可知生成的二氧化碳________g。
②参加反应的碳酸钙质量多少_______?
③该实验所得石灰石中碳酸钙的含量偏小,原因是_____________(多选)。
A 产生的气体残留在装置中
B 氢氧化钠溶液中氢氧化钠含量不足
C 被吸收的气体含有原装置空气中的二氧化碳
【答案】2.2 5g AB
【解析】
①根据质量守恒定律可知,生成的二氧化碳的质量为2.2g;
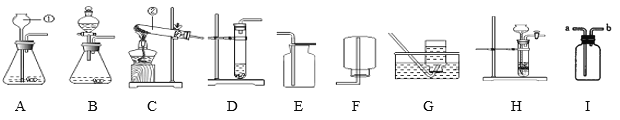
②设碳酸钙的质量为x,则
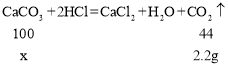
![]()
解得x=5g;
③造成碳酸钙含量偏低应该考虑二氧化碳的未完全吸收,所以产生气体残留在装置内会造成偏小,同样氢氧化钠的质量偏小也会造成二氧化碳不能被完全吸收而偏小;故选:AB。

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目