题目内容
下列现象中,与蜡烛燃烧时所观察到的现象不符的是:
- A.发出黄白色的火焰
- B.火焰上方如果罩一干燥烧杯时能发现烧杯内壁上有水珠
- C.蜡烛靠近火焰处熔化变成液体
- D.蜡烛燃烧时浓烟滚滚
D
A、蜡烛燃烧时发出亮黄色的光,故A说法符合观察现象;
B、在蜡烛火焰上方罩一干燥烧杯,能发现烧杯内壁上有水珠出现,故B说法符合观察现象;
C、蜡烛靠近火焰处熔化变成液体,故C说法符合观察现象;
D、点燃蜡烛能持续燃烧,有少量黑烟,故D说法不符合观察现象;
故选D.
A、蜡烛燃烧时发出亮黄色的光,故A说法符合观察现象;
B、在蜡烛火焰上方罩一干燥烧杯,能发现烧杯内壁上有水珠出现,故B说法符合观察现象;
C、蜡烛靠近火焰处熔化变成液体,故C说法符合观察现象;
D、点燃蜡烛能持续燃烧,有少量黑烟,故D说法不符合观察现象;
故选D.

练习册系列答案
相关题目
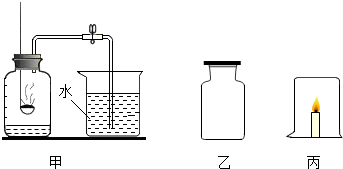
 (2012?宣城模拟)有一种神奇的蜡烛,点燃后任你怎么吹也吹不灭,而且看上去和普通的蜡烛一模一样,那么到底是什么玄机能让蜡烛持续燃烧?请你一起参与探究.
(2012?宣城模拟)有一种神奇的蜡烛,点燃后任你怎么吹也吹不灭,而且看上去和普通的蜡烛一模一样,那么到底是什么玄机能让蜡烛持续燃烧?请你一起参与探究.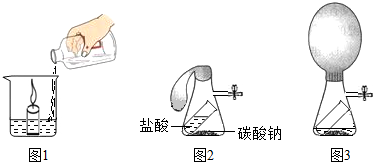
 (2012?乐陵市一模)有一种神奇的蜡烛,点燃后任你怎么吹也吹不灭,而且看上去和普通的蜡烛一模一样,那么到底是什么玄机能让蜡烛持续燃烧?请你一起参与探究.
(2012?乐陵市一模)有一种神奇的蜡烛,点燃后任你怎么吹也吹不灭,而且看上去和普通的蜡烛一模一样,那么到底是什么玄机能让蜡烛持续燃烧?请你一起参与探究.