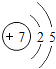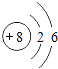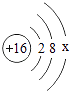题目内容
【题目】了解物质的结构,有利于理解和认识化学问题.
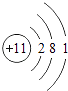
(1)下表为部分元素的原子结构示意图:
元素名称 | 氢 | 氦 | 氮 | 氧 | 钠 | 硫 |
元素符号 | H | He | N | O | Na | S |
原子结构示意图 |
|
|
|
|
|
|
请回答下列问题:
①表中硫原子的最外层电子数x=;若x=8,请写出该粒子的符号 .
②表中具有相对稳定结构的原子是(填符号).
③钠与硫反应过程中,钠原子因失去最外层1个电子达到相对稳定结构,显+1价.试解释NaH中H显﹣l价的原因
④上述元素组成的酸有多种,试写出由三种元素组成的酸的化学式(任写一种).
(2)高温条件下,NH3在O2中用铂一铑合金(Pt﹣Rh)催化氧化.若催化机理如图所示:试写出该反应的化学方程式 
【答案】
(1)6;S2﹣;He;化学变化中一个氢原子要得到一个电子而达到稳定结构;HNO3
(2)4NH3+5O2 ![]() 4NO+6H2O
4NO+6H2O
【解析】解:(1)①原子中质子数等于核外电子数,所以16=2+8+x,x=6,若x=8,则核外电子数比核内质子数多2,该离子带两个单位的负电荷离子符号为S2﹣;②根据稳定结构的原子一般是指最外层电子数是8(氦是2)的原子;观察图示的微粒结构可知He属于稳定结构的原子;③因为钠与硫反应过程中,钠原子因失去最外层1个电子达到相对稳定结构,显+1价,而NaH中氢原子得到一个电子而达到稳定结构,所以氢元素显﹣1价;④根据表中的有关元素情况可知由三种元素组成的酸的化学式可以是HNO3、H2SO4等;(2)根据反应的过程可以看出反应前是4个NH3分子和5个O2分子,而反应最终是4个NO分子和6个H2O分子,所以该反应的方程式为4NH3+5O2 ![]() 4NO+6H2O; 所以答案是:(1)①6;S2﹣;②He;③化学变化中一个氢原子要得到一个电子而达到稳定结构;④HNO3;(2)4NH3+5O2
4NO+6H2O; 所以答案是:(1)①6;S2﹣;②He;③化学变化中一个氢原子要得到一个电子而达到稳定结构;④HNO3;(2)4NH3+5O2 ![]() 4NO+6H2O;
4NO+6H2O;
【考点精析】认真审题,首先需要了解书写化学方程式、文字表达式、电离方程式(注意:a、配平 b、条件 c、箭号).