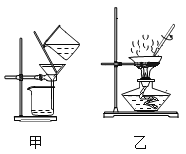
题目内容
【题目】元素周期律和周期表是学习化学的重要工具,下表是元素周期表的部分信息。
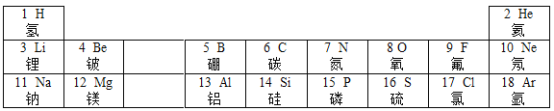
请认真分析表中信息,回答下列问题:
(1)地壳中含量仅次于氧的非金属元素名称是_____,该元素原子的质子数为_____。
(2)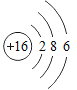 所表示的粒子符号为_____,它的最外层电子数为_____。
所表示的粒子符号为_____,它的最外层电子数为_____。
(3)由原子序数为8和13的两种元素组成的化合物是_____(写化学式)。
(4)元素周期表同一横行元素的排列规律是:从左至右_____。
(5)表中不同种元素最本质的区别是_____(填序号):
A 质子数不同
B 中子数不同
C 相对原子质量不同
【答案】硅 14 S 6 Al2O3 由金属元素逐渐过渡到非金属元素,最后以稀有气体元素结尾;或原子的最外层电子数由1逐渐增加到8 A
【解析】
(1)地壳中元素含量由多到少的顺序是氧、硅、铝、铁等,故仅次于氧的非金属元素名称是硅,该元素原子的质子数为14。
(2)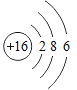 所表示的粒子质子数为16,该元素是硫元素,符号为S,它的最外层电子数为6。
所表示的粒子质子数为16,该元素是硫元素,符号为S,它的最外层电子数为6。
(3)原子序数为8和13的两种元素分别是氧、铝,它们组成的化合物是Al2O3。
(4)元素周期表同一横行元素的排列规律是:从左至右由金属元素逐渐过渡到非金属元素,最后以稀有气体元素结尾(或原子的最外层电子数由1逐渐增加到8)。
(5)元素是具有相同核电荷数的一类原子的总称,表中不同种元素最本质的区别是质子数不同,故选A。

练习册系列答案
相关题目
【题目】有A、B、C三种元素,它们形成的粒子结构示意图如下,其中说法正确的是( )
元素 | A | B | C |
其形成的粒子结构示意图 |
|
|
|
A. 它们之间可形成化学式为AC的化合物
B. 它们原子的核外电子层数相同
C. A的粒子结构示意图表示的是原子, B、C表示的是阳离子
D. 它们之间可形成化学式为B2A的化合物