题目内容
【题目】如图1所示,A、B、C为三种物质的溶解度曲线,请根据图示信息回答下列问题. 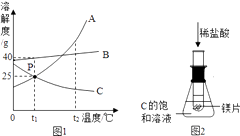
(1)t1℃时,100克A的饱和溶液中含溶质的质量是 .
(2)t1℃时,将30g B物质投入100g水中,充分溶解,温度不变,所得溶液为溶液(填“饱和”或“不饱和”)
(3)下列说法正确的是 .
A.t2℃时,将A和C的混合溶液(两者均已达到饱和),降温至t1℃,析出晶体含有A和C
B.t2℃,将A,B,C的饱和溶液分贝降温至t1℃,所得溶液中溶质质量分数的大小关系是B>A>C
C.从混有少量A的C物质中提取较纯净的C,可通过升温结晶的方法来实现
D.t1℃时,欲用A的饱和溶液配制10%的A溶液,只需要烧杯、量筒、胶头滴管三种玻璃仪器
(4)如图2所示,向放有镁片的试管中滴加稀盐酸后,锥形瓶中C中的饱和溶液变浑浊,请解释原因 .
【答案】
(1)20g
(2)不饱和
(3)BC
(4)镁与盐酸反应放出热量导致温度升高,C的溶解度减小
【解析】解:(1)t1℃时,A物质的溶解度是25g,所以100克A的饱和溶液中含溶质的质量是 ![]() ×100%×100g=20g;(2)t1℃时,B的溶解度是40g,将30gB物质投入100g水中,充分溶解,温度不变,所得溶液为不饱和溶液;(3)A.t2℃时,将A和C的混合溶液(两者均已达到饱和),降温至t1℃,C的溶解度随温度的降低而减小,故C无晶体析出,故A错误;B.由于在t2℃时,三物质的溶解度的大小关系为A>B>C,则其饱和溶液中溶质的质量分数的大小关系为A>B>C,将三种物质的饱和溶液将温到t1℃时,由于A和B的溶解度都随温度的降低而减小,它的溶液中就会有晶体析出,溶液中溶质的质量分数就会减小,但C的溶解度随温度的降低而增大,因此溶液中溶质的质量分数都不发生变化,但由图不难看出三物质的溶解度的大小关系为B>A>C,所得溶液中溶质质量分数的大小关系是B>A>C,故B正确;
×100%×100g=20g;(2)t1℃时,B的溶解度是40g,将30gB物质投入100g水中,充分溶解,温度不变,所得溶液为不饱和溶液;(3)A.t2℃时,将A和C的混合溶液(两者均已达到饱和),降温至t1℃,C的溶解度随温度的降低而减小,故C无晶体析出,故A错误;B.由于在t2℃时,三物质的溶解度的大小关系为A>B>C,则其饱和溶液中溶质的质量分数的大小关系为A>B>C,将三种物质的饱和溶液将温到t1℃时,由于A和B的溶解度都随温度的降低而减小,它的溶液中就会有晶体析出,溶液中溶质的质量分数就会减小,但C的溶解度随温度的降低而增大,因此溶液中溶质的质量分数都不发生变化,但由图不难看出三物质的溶解度的大小关系为B>A>C,所得溶液中溶质质量分数的大小关系是B>A>C,故B正确;
C.A的溶解度受温度影响变化较大,从混有少量B的A物质中提取较纯净的A,可通过降温结晶的方法实现,故C正确;
D.t1℃时,欲用A的饱和溶液配制10%的A溶液,需要烧杯、量筒、胶头滴管、玻璃棒四种玻璃仪器,故D错误;
故选:BC;(4)向放有镁片的试管中滴加稀盐酸后,锥开瓶中C中的饱和溶液变浑浊,原因在于镁与盐酸反应放出了热量,温度升高,而C的溶解度随温度的升高而减小.
所以答案是:(1)20g;(2)不饱和;(3)BC;(4)镁与盐酸反应放出热量导致温度升高,C的溶解度减小.
【考点精析】解答此题的关键在于理解固体溶解度曲线及其作用的相关知识,掌握1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和).

