题目内容
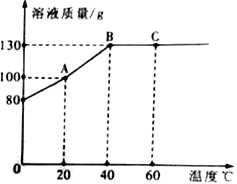
为了测量大理石中碳酸钙的含量,小明将质量为12.5克的大理石放入锥形瓶中,在锥形瓶中不断加入一定浓度的稀盐酸(如图甲),读出电子天平的示数,绘出所加稀盐酸的质量和锥形瓶中物质的质量关系图乙所示。(已知:CaCO3+2HCl=CaCl2+H2O+CO2↑,样品中杂质不与稀盐酸反应,实验前后锥形瓶中气体质量的变化忽略不计)

(1)在不断加入稀盐酸的过程中,我们通过观察图甲装置中哪一现象即可判断大理石已经反应完全___?
(2)求大理石中碳酸钙的质量分数______。
(3)由图乙可知,加入等质量的稀盐酸,ab阶段锥形瓶中增加的物质质量小于bc阶段原因是___。
小军同学在学习酸碱盐有关知识时,对一些沉淀物质的颜色产生了兴趣。老师告诉他氢氧化铜是蓝色、氢氧化铁是红褐色,让他自己探究氢氧化亚铁的颜色。下面请你和他一起探究。
[查阅资料]:(1)铁有两种氢氧化物,它们可以分别由相对应的可溶性盐与碱溶液反应而制得。
(2)氢氧化亚铁在空气中立即被氧化。
(3)硫酸铜溶液是蓝色,硫酸亚铁溶液是浅绿色。
[提出猜想]:氧化亚铁是浅绿色。
[实验过程]:在2支试管里分别加入少量FeCl3和FeSO4溶液,然后滴入NaOH溶液,观察现象。请补充完成下表:
2支试管里分别加入少量FeCl3和FeSO4溶液,然后滴入NaOH溶液,观察现象。请补充完成下表:
FeCl3溶液 | FeSO4溶液 | |
滴入NaOH溶液的现象 | 生成红褐色沉淀 | 先生成白色絮状沉淀,迅速变成灰绿色,最后变成红褐色沉淀。 |
化学方程式 | 基本反应类型属于_____反应。 | FeSO4+2NaOH=Fe(OH)2↓Na2SO4 Fe(OH)2+_____+_____H2O=_____ (完成并配平此方程) |
[学习交流]:(1)氢氧化亚铁是_____色而不是浅绿色。
(2)小军联系到CO2与C的反应,认为FeCl3溶液可以转化为FeCl2溶液。你认为小军的理由是_____。
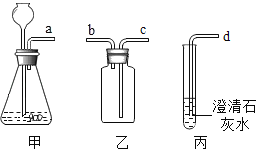
实验室利用下列装置收集并检验二氧化碳进行相关实验。请按要求回答问题:
指示剂 | 酸性 | 中性 | 碱性 |
菊花浸出液 | 红色 | 紫色 | 黄色 |
(1)利用乙收集二氧化碳气体,应从___端通入。(填字母)
(2)正确连接甲、乙、丙装置后,当观察到丙装置出现___现象时,说明乙装置中二氧化碳气体收集满了。
(3)上表是菊花浸出液在不同条件下的显色情况。若将丙试管中的澄清石灰水换成菊花浸出液,将二氧化碳通入丙装置后,观察到菊花浸出液变为红色,其原因是___。