题目内容
【题目】几年前,我国南方地区遭受了一场特大雪灾,道路结冰,给交通带来极大不便.为了快速消除道路上的积雪,交通部门使用了大量的融雪剂,某公司生产的融雪剂是由NaCl、CaCl2、Na2CO3和CuSO4中的一种或两种物质组成.化学兴趣小组的小红和小兰对
步骤 | 操作 | 现象 |
Ⅰ | 加水溶解 | 得无色澄清溶液 |
Ⅱ | 加入Na2CO3溶液 | 生成白色沉淀 |
融雪剂产生很大的兴趣并对融雪剂的成分进行积极的探究.
[探究实验一]取一定量的融雪剂分装两支试管,进行如下实验,现象记录如下:
(1)【分析思考】融雪剂中一定含有 , 一定不含有、 . 由此看初步确定其成分有两种可能性:① , ② .
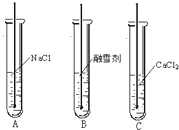
(2)【探究实验二】为了进一步确定该融雪剂的成分,小红、小兰查阅资料得知氯化钙溶于水会放热,氯化钠溶于水温度几乎不变.根据不同物质溶于水时的温度变化不同设计了如下实验:将等质量的NaCl固体、融雪剂、CaCl2固体分别溶于等体积的水中,并用温度计测定溶液的温度,装置如上图所示.
小红、小兰预测:若装置B中温度计的读数介于装置A、C中温度计的读数之间,则可确定融雪剂的成分为 . (用化学式表示)实际操作中,测得A、B、C三个装置中温度计的读数非常接近,没有达到预期的结果.试分析实验失败的原因可能是 . (只写一方面的原因即可)
【答案】
(1)CaCl2;CuSO4;Na2CO3;CaCl2;NaCl、CaCl2
(2)NaCl、CaCl2;三种固体的质量取得不足或取用的水过多
【解析】解:【分析思考】由于含铜离子的盐溶液呈蓝色,又由于融雪剂溶于水得无色澄清溶液,因此由得无色溶液可以确定融雪剂中一定不含硫酸铜;
由于融雪剂中加入碳酸钠溶液生成白色沉淀,可以确定融雪剂中一定含有钙离子,即一定含有氯化钙.由于钙离子与碳酸根离子作用会形成碳酸钙白色沉淀,因此由得澄清溶液可以确定融雪剂中一定不含碳酸钠.故融雪剂可能是只含有氯化钙或是含有氯化钙和氯化钠;
【探究实验二】由于氯化钙溶于水会放出大量的热,氯化钠溶于水不放出热,因此可以由“装置B中温度计的读数介于装置A、C中温度计的读数之间”确定融雪剂的成分为NaCl和CaCl2 .
实际操作中,测得A、B、C三个装置中温度计的读数非常接近,没有达到预期的结果.实验失败的原因可能是两种固体取得太少或是水的量取的太多等.
所以答案是:CaCl2;Na2CO3 CuSO4;①CaCl2;②NaCl、CaCl2
NaCl、CaCl2;三种固体的质量取得不足或取用的水过多.
【考点精析】认真审题,首先需要了解溶解时的吸热或放热现象(溶解时放热、吸热现象<溶解吸热:如NH4NO3溶解;溶解放热:如NaOH溶解、浓H2SO4溶解;解没有明显热现象:如NaCl>).

 阅读快车系列答案
阅读快车系列答案
