题目内容
用下图装置测定因存放不当而部分变成碳酸钠的烧碱中氢氧化钠的质量分数.所取试样质量8.00 g、锥形瓶质量140.00 g,加入足量稀硫酸(质量为50.00 g)每隔相同时间读数一次,数据如下表:
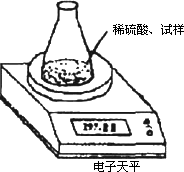

(1)不必进行第七次读数的原因是________.
(2)计算氢氧化钠的质量分数.
(3)所用稀硫酸中H2SO4的质量分数不低于多少?
解析:
|
解:(1)第5次和第6次读数相同,说明已充分反应; (2)CO2的质量m(CO2)=(8.00 g+140.00 g+50.00 g)-197.12 g=0.88 g 设所需样品中Na2CO3的质量为x Na2CO3+H2SO4=H2O+CO2↑+Na2SO4 106 44 x 0.88 g x=(0.88×106)/44=2.12 g 则所取样品中NaOH的质量分数为:(5.88/9.00)×100%=73.5% (3)设样品中Na2CO3消耗H2SO4的质量为y Na2CO3+H2SO4=H2O+CO2↑+Na2SO4 106 98 2.12 g y Y=(2.12 g×98)/106=1.96 g 再设试样中NaOH消耗H2SO4的质量为z 2NaOH+H2SO4=Na2SO4+2H2O 80 98 5.88 g z z=(5.88 g×98)/80=7.20 g 则稀硫酸中H2SO4的质量分数不低于[(1.96 g+7.20 g)/50.00 g]×100%=18.32% 答:略 |

 全能测控期末小状元系列答案
全能测控期末小状元系列答案用下图装置测定因存放不当而部分变成碳酸钠的烧碱的质量分数,所取试样质量:8.OOg、锥形瓶质量140.OOg,加入足量稀硫酸(质量为5O.OOg)每隔相同时间读数一次,数据如下表:
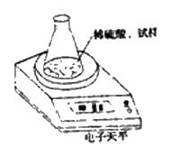
| 读数次数 | 质量/g | |
| 锥形瓶 +试剂+ 稀硫酸 | 第1次 | 197.64 |
| 第2次 | 197.48 | |
| 第3次 | 197.26 | |
| 第4次 | 197.16 | |
| 第5次 | 197.12 | |
| 第6次 | 197.12 |
(1)不必进行第七次读数的原因是________________。
(2)计算氢氧化钠的质量分数.
(3)所用稀硫酸中硫酸的质量分数不低于多少?
