��Ŀ����
����Ŀ��������(Na2SiO3)���ҹ����ȷ�չ�ľ�ϸ��ѧƷ����ij��ʯӢɰ��ʯ(��Ҫ�ɷ���SiO2��������������CuO��Na2SO4��Na2CO3)�Ʊ�������(Na2SiO3)���������£�
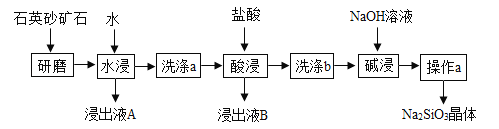
���ϣ�SiO2�Ȳ�����ˮ��Ҳ�������ᷴӦ��
���ʴ��������⣺
(1)����ĥ����Ŀ����_______ ��
(2)������ϴ��a����ϴ���ķ�����____________��
(3)��������Ļ�ѧ����ʽΪ____________��
(4)��������Ļ�ѧ����ʽΪ____________��
(5)������a����������Ũ����_____ �����ˡ�ϴ�ӡ������һϵ�в�����
���𰸡� ʹ�ܽ���߷�Ӧ��������� ȡ���˵õ�����Һ�����Ȼ�����Һ������������ CuO+H2SO4=CuSO4+H2O SiO2+2NaOH=H2O+Na2SiO3 ���½ᾧ
��������(1)���ڷ�Ӧ��֮��Ӵ�Խ��ַ�ӦԽ�죬ͬʱ����ԽС���ܽ�Ҳ��Խ�죬��������ĥ����Ŀ���� ʹ�ܽ���߷�Ӧ��������ף�(2)������ϴ��a����ϴ������˵�������ϴ��Һ��û�����ɵ�̼���ƺ������ƣ����Ծ��Ǽ����Ƿ��в�����̼���ƺ������ƣ����Է����� ȡ���˵õ�����Һ�����Ȼ�����Һ������������(3)��������dz�ȥ����ͭ��������ͭ�����ᷴӦ��������ͭ��ˮ����Ӧ�Ļ�ѧ����ʽΪ CuO+H2SO4=CuSO4+H2O��(4)��������Ƕ���������������Ʒ�Ӧ�����ɹ����ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪ SiO2+2NaOH=H2O+Na2SiO3��(5)������a����������Ũ�������½ᾧ�����ˡ�ϴ�ӡ������һϵ�в�����

 ��У����ϵ�д�
��У����ϵ�д�