题目内容
碳酸钠和氯化钠的混合物14g,常温下溶解在87g水中;向溶液中逐滴加入氯化钙溶液.加入氯化钙溶液的质量与生成的沉淀质量的关系如下图:
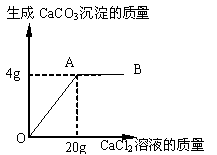
(1)图像中表示恰好完全反应的点是__________________;
(2)求原混合物中氯化钠的质量分数;
(3)求恰好完全反应时溶液中溶质的质量分数.
(2)求原混合物中氯化钠的质量分数;
(3)求恰好完全反应时溶液中溶质的质量分数.
(1)A
(2)设原混合物中碳酸钠的质量为xg,生成氯化钠的质量为yg。
Na2CO3+CaCl2===CaCO3↓+2NaCl
106 100 117
x 10g y
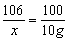
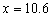 g
g
14g-10.6g=3.4g
原混合物中的质量为: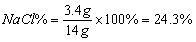
(3)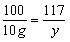
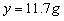
反应后溶液中NaCl的质量:14g+60g+87g-10g=151g
恰好反应时溶质的质量:11.7g+(14g-10.6g)=15.1g
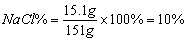
答:(2)原混合物中氯化钠的质量分数为24.3%
(3)恰好完全反应时溶液中溶质的质量分数为10%
(2)设原混合物中碳酸钠的质量为xg,生成氯化钠的质量为yg。
Na2CO3+CaCl2===CaCO3↓+2NaCl
106 100 117
x 10g y
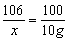
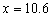 g
g14g-10.6g=3.4g
原混合物中的质量为:
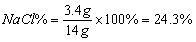
(3)
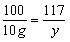
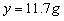
反应后溶液中NaCl的质量:14g+60g+87g-10g=151g
恰好反应时溶质的质量:11.7g+(14g-10.6g)=15.1g
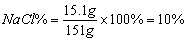
答:(2)原混合物中氯化钠的质量分数为24.3%
(3)恰好完全反应时溶液中溶质的质量分数为10%

练习册系列答案
相关题目
 (2013?泰安)小明在协助老师清理实验室时,发现有一瓶碳酸钠和氯化钠组成的混合液.他想测定该溶液中碳酸钠和氯化钠的质量分数,为此设计并进行了如下实验.
(2013?泰安)小明在协助老师清理实验室时,发现有一瓶碳酸钠和氯化钠组成的混合液.他想测定该溶液中碳酸钠和氯化钠的质量分数,为此设计并进行了如下实验.