题目内容
(2004?厦门)据国家标准,碳铵化肥的NH4HCO3含量不得低少于95%.陈红同学利用图装置和如下反应进行了三次实验,且假设杂质不发生反应.NH4HCO3=NH3↑+H2O+CO2↑;2NH3+H2SO4═(NH4)2SO4.实验结果如下:
| 实验次数 | 1 | 2 | 3 | 平均值 |
| 使用样品的质量(克) | 8.00 | 8.00 | 8.00 | 8.00 |
| 硫酸溶液增加的质量(克) | 1.71 | 1.69 | 1.70 | 1.70 |
(2)这个结果能否说明这种化肥合格与否,请说明原因.

【答案】分析:(1)假设硫酸溶液增加的质量全是氨气的质量,根据碳酸氢铵分解的化学方程式和氨气的质量,列出比例式,即可计算出参与反应的NH4HCO3质量,然后再根据质量分数公式就可计算出该化肥中碳酸氢铵的百分含量;
(2)根据浓硫酸的性质,即可说明原因.
解答:解:(1)设参与反应的NH4HCO3质量为x,
NH4HCO3=NH3↑+H2O+CO2↑
79 17
x 1.7g
79:17=x:1.7g
解之得:x=7.9g;
该化肥中碳酸氢铵的质量分数为: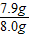 ×100%=98.75%;
×100%=98.75%;
(2)这个结果不能说明这种化肥合格,因为浓硫酸有吸水性,在陈红同学的实验中,浓硫酸增加的质量,不一定全部是吸收氨气的质量,也可能还有水的质量.
点评:本题主要考查考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.
(2)根据浓硫酸的性质,即可说明原因.
解答:解:(1)设参与反应的NH4HCO3质量为x,
NH4HCO3=NH3↑+H2O+CO2↑
79 17
x 1.7g
79:17=x:1.7g
解之得:x=7.9g;
该化肥中碳酸氢铵的质量分数为:
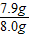 ×100%=98.75%;
×100%=98.75%;(2)这个结果不能说明这种化肥合格,因为浓硫酸有吸水性,在陈红同学的实验中,浓硫酸增加的质量,不一定全部是吸收氨气的质量,也可能还有水的质量.
点评:本题主要考查考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
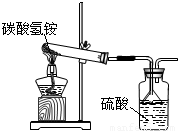
(2004?厦门)据国家标准,碳铵化肥的NH4HCO3含量不得低少于95%.陈红同学利用图装置和如下反应进行了三次实验,且假设杂质不发生反应.NH4HCO3=NH3↑+H2O+CO2↑;
2NH3+H2SO4═(NH4)2SO4.实验结果如下:
(1)陈红认为硫酸溶液增加的质量是氨气(NH3)的质量,根据陈红的分析,请利用实验平均值计算出该化肥中碳酸氢铵的百分含量.
(2)这个结果能否说明这种化肥合格与否,请说明原因.
2NH3+H2SO4═(NH4)2SO4.实验结果如下:
| 实验次数 | 1 | 2 | 3 | 平均值 |
| 使用样品的质量(克) | 8.00 | 8.00 | 8.00 | 8.00 |
| 硫酸溶液增加的质量(克) | 1.71 | 1.69 | 1.70 | 1.70 |
(2)这个结果能否说明这种化肥合格与否,请说明原因.

(2004?厦门)据国家标准,碳铵化肥的NH4HCO3含量不得低少于95%.陈红同学利用图装置和如下反应进行了三次实验,且假设杂质不发生反应.NH4HCO3=NH3↑+H2O+CO2↑;
2NH3+H2SO4═(NH4)2SO4.实验结果如下:
(1)陈红认为硫酸溶液增加的质量是氨气(NH3)的质量,根据陈红的分析,请利用实验平均值计算出该化肥中碳酸氢铵的百分含量.
(2)这个结果能否说明这种化肥合格与否,请说明原因.

2NH3+H2SO4═(NH4)2SO4.实验结果如下:
| 实验次数 | 1 | 2 | 3 | 平均值 |
| 使用样品的质量(克) | 8.00 | 8.00 | 8.00 | 8.00 |
| 硫酸溶液增加的质量(克) | 1.71 | 1.69 | 1.70 | 1.70 |
(2)这个结果能否说明这种化肥合格与否,请说明原因.

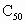 颗粒.1985年美国科学家斯莫利发现了
颗粒.1985年美国科学家斯莫利发现了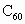 ,获得了1996年诺贝尔化学奖.
,获得了1996年诺贝尔化学奖.
 都是由碳原子构成的,它们是相同的一种物质
都是由碳原子构成的,它们是相同的一种物质