题目内容
【题目】(7分)某化学兴趣小组在探究稀盐酸的化学性质时,做了如图一所示的三个实验。
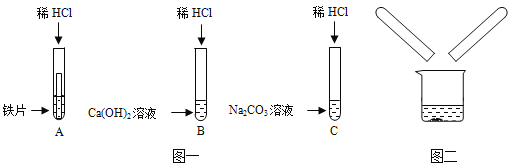
(1)写出A试管中的反应现象 。
(2)写出B试管中反应的化学方程式 。
(3)实验结束后,小组同学将B、C两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成。同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究。
【提出猜想】
甲同学猜想:NaCl;
乙同学猜想:NaCl、CaCl2;
丙同学猜想:NaCl、CaCl2、 HCl;
你的猜想: 。
【交流讨论】
你认为 同学的猜想一定不正确,理由是 。
【设计实验】请设计实验证明你的猜想正确。
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,向其中滴加 。 | 猜想成立 |
【答案】(1)铁片表面有气泡产生,溶液由无色逐渐变为浅绿色
(2)Ca(OH)2+2HCl===CaCl2+2H2O
(3)你的猜想:NaCl、Na2CO3
①丙 理由是:白色沉淀是CaCO3,能与盐酸反应,二者不能共存(表述合理即可)
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,向其中滴加 无色酚酞试液 。 | 无色酚酞试液变红 | 猜想成立 |
(或滴加紫色石蕊试液,实验现象为紫色石蕊试液变蓝;滴加稀盐酸等稀酸,实验现象为产生气泡;滴加CaCl2溶液、BaCl2溶液、Ca(NO3)2溶液、Ba(NO3)2溶液、Ca(OH)2溶液、Ba(OH)2溶液,实验现象为产生白色沉淀等合理即可,但要注意所加试剂与实验现象相对应。)
【解析】
试题分析:(1)铁和稀盐酸反应生成的是氯化亚铁和氢气,现象是铁片表面有气泡产生,溶液由无色逐渐变为浅绿色;
(2)氢氧化钙和稀盐酸反应生成的是氯化钙和水:Ca(OH)2+2HCl===CaCl2+2H2O;
(3)C试管中发生的反应是碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳。将B、C两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成,说明B试管中的稀盐酸过量,C试管中的碳酸钠过量,稀盐酸先与碳酸钠反应生成氯化钠、水和二氧化碳,然后氯化钙与碳酸钠反应生成碳酸钙沉淀和氯化钠。故将烧杯内的物质进行过滤,所得滤液的溶质成分可能是氯化钠或氯化钠、氯化钙或氯化钠、碳酸钠。由于最后生成了白色沉淀,故不可能含有稀盐酸;
要证明溶液中含有碳酸钠,可向溶液滴加无色酚酞或紫色石蕊或滴加稀盐酸等。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案【题目】下列除杂质的方法不正确的是
选项 | 物质(括号内为杂质) | 除杂方法 |
A | NaCl(Na2CO3) | 加入足量稀盐酸,蒸发结晶 |
B | KCl(MnO2) | 溶解,过滤,蒸发结晶 |
C | CO2(CO) | 在空气中点燃 |
D | Cu (Fe) | 加入足量的稀盐酸,过滤 |