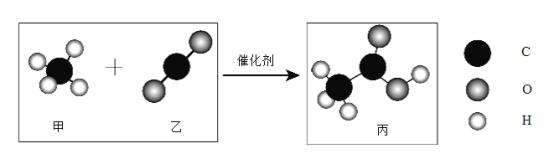
题目内容
化学课上同学们进行实验验证酸的性质。
I. 与指示剂作用。

(1)在白色点滴板孔穴1、3中加入紫色石蕊溶液,观察到溶液变_____色。
(2)将无色酚酞溶液滴加到孔穴2、4中,观察到孔穴4中溶液为无色,而孔穴2中溶液变为橙色。同学们猜想孔穴2中的异常现象与硫酸溶液的浓度过高有关,并通过以下实验证明该猜想正确:取少量上述橙色溶液于试管中,加水稀释,观察到的现象是_____。
II. 与铁锈反应。
实验 | 实验试剂 | 实验现象 |
1 | 锈蚀铁钉+10 mL 稀盐酸 | 生成无色气泡,铁锈较快消失,溶液颜色变黄。 |
2 | 锈蚀铁钉+10 mL 稀硫酸 | 生成无色气泡,铁锈减少速度缓慢,溶液颜色未变黄。 |
(提出问题)实验1、2现象不同的原因是什么?
(查阅资料)HCl在水中会解离出H+和Cl-,H2SO4在水中会解离出H+和SO42-。
(假设猜想)可能和溶液中阴离子不同有关。
(进行实验)
实验 | 实验试剂 | 实验现象 |
3 | 锈蚀铁钉+10 mL稀硫酸 + _A_ | 生成无色气泡,铁锈减少速度比实验2快,溶液颜色变黄。 |
4 | 锈蚀铁钉+10 mL稀盐酸 + Na2SO4 | 生成无色气泡,铁锈减少速度比实验1慢,溶液颜色变黄。 |
(解释和结论)
(3)铁锈(主要成分为Fe2O3)和盐酸反应的化学方程式是_____。
(4)实验1中产生的无色气体是_____。
(5)实验3中,物质A是_____。
(6)结合实验1~4,得出的结论是_____。
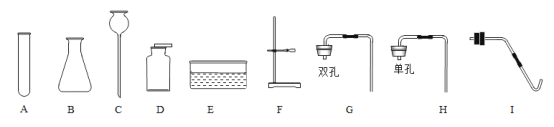
请从A或B中任选一个作答,若两题均作答,按A计分。

A | B |
(1)用高锰酸钾制取氧气,发生装置应选取_____(填序号),该反应的化学方程式为_____。 (2)用C装置收集氧气时,验满的操作是_____。 | (1)用过氧化氢和二氧化锰制取氧气,发生装置应选取_____(填序号),该反应的化学方程式为_____。 (2)可用E装置收集氧气的原因是_____。 |