题目内容
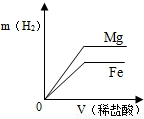
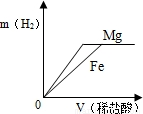
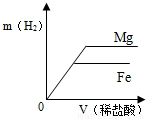
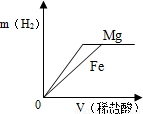
相同质量的Mg、Fe分别与稀盐酸作用,产生H2的质量m(H2)与加入稀盐酸的体积V(稀盐酸)关系如下图所示,其中正确的是( )A.
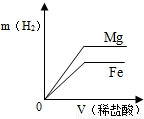
B.

C.

D.

【答案】分析:由于两种金属都能和盐酸反应,但是当相等质量的金属完全反应时得到的氢气不同.但是当酸的质量相同时,生成的氢气应该是相等的.(本题不要考虑金属活动的强弱,也就是不要理解坡度越大,金属越活泼,因为横坐标不是时间,而是盐酸的体积)
解答:解:由于两种金属都能够与盐酸反应,所以都能得到气体.当相同质量的金属完全反应时,得到的氢气应该是镁对应的更多,这样就排除了BC.同时当加入的酸不能将金属完全反应时,也就是金属完全反应之前,消耗等量的酸则对应等量的氢气生成,所以在其中金属完全反应掉之前,两金属的曲线是重合的.当由于金属完全反应时,铁消耗的盐酸的质量小,所以就先完全反应,且得到氢气要少.而镁继续反应至完全反应,这样消耗的酸多,对应的氢气也多.则为D.
故选D
点评:本题考查了金属与酸反应及产生氢气质量的关系,完成此题,可以依据已有的知识.所以要求同学们在平时的学习中加强基础知识的记忆和理解,以便能够灵活应用.(本题切勿陷入金属越活泼,反应越快的思维误区)
解答:解:由于两种金属都能够与盐酸反应,所以都能得到气体.当相同质量的金属完全反应时,得到的氢气应该是镁对应的更多,这样就排除了BC.同时当加入的酸不能将金属完全反应时,也就是金属完全反应之前,消耗等量的酸则对应等量的氢气生成,所以在其中金属完全反应掉之前,两金属的曲线是重合的.当由于金属完全反应时,铁消耗的盐酸的质量小,所以就先完全反应,且得到氢气要少.而镁继续反应至完全反应,这样消耗的酸多,对应的氢气也多.则为D.
故选D
点评:本题考查了金属与酸反应及产生氢气质量的关系,完成此题,可以依据已有的知识.所以要求同学们在平时的学习中加强基础知识的记忆和理解,以便能够灵活应用.(本题切勿陷入金属越活泼,反应越快的思维误区)

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目