题目内容
重庆一中化学兴趣小组的同学将氢氧化钠溶液和稀硫酸混合,没有观察到明显的现象,他们对此提出了如下问题并进行了相应探究:
问题一:二者之间是否发生了反应?他们设计了如下方案证明二者之间确实发生了反应:
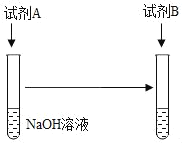
(1)可以选择的试剂组合有_____(填序号)。
①试剂 A:足量稀硫酸,试剂 B:MgCl2溶液
②试剂 A:足量稀硫酸,试剂 B:铁粉
③试剂 A:少量稀硫酸,试剂 B:MgCl2溶液
④试剂 A:少量稀硫酸,试剂 B:铁粉
(2)小兰认为,若选用_____溶液,不管加入顺序如何,只需控制加入稀硫酸的量也 能证明二者发生了反应。
问题二:反应后溶液中溶质有哪些?
(猜想假设)猜想一:只有 Na2SO4;猜想二:Na2SO4 和_____;猜想三:Na2SO4 和 H2SO4。
(查阅资料)①Na2SO4 溶液显中性,②Na2SO4+BaCl2=BaSO4↓+2NaCl。
(实验操作)分别取少量反应后的溶液于试管中,进行如下实验:
实验编号 | 实验过程 | 实验现象 |
① | 加入酚酞溶液 | 不变红 |
② | 加入少量 BaCl2溶液 | 产生白色沉淀 |
③ | 加入少量 Na2CO3溶液 | _____(填“有”或“无”)气泡产生 |
(实验结论)猜想一成立。
(实验反思)小娜认为,实验_____(填实验编号)可省略。 小秋用精密仪器检测反应后溶液中离子的个数比,也得出了相同结论,则测得溶液中的 Na+和 SO42﹣个数比为_____。
下列实验操作对应的现象与结论均正确的是( )
实验操作 | 现象 | 结论 | |
A | 用拇指堵住H2的试管口,靠近火焰,移开拇指点燃 | 发出尖锐爆鸣声 | 试管中H2是纯净的 |
B | 往久置在空气中的NaOH溶液中滴加稀H2SO4 | 产生大量气泡 | NaOH溶液已变质 |
C | 把质量相同的Mg条与Fe片同时放入相同浓度和体积的稀 HCl中 | Mg条产生气体快 | Mg的金属活动性比Fe强 |
D | 往无色溶液中滴加BaCl2溶液 | 产生白色沉淀 | 无色溶液中一定含有SO42﹣ |
A. A B. B C. C D. D
化学是以实验为基础的学科,根据下列实验回答问题。
实验一 | 实验二 | 实验三 |
|
|
|
(1)实验一:待红磷熄灭冷却后,打开弹簧夹,观察到集气瓶内水面上升约______。该实验现象说明氮气具有的性质是不可燃、不助燃以及____。
(2)实验二:三天后,观察到序号为____的试管中的铁钉明显生锈。对照实验②和③,可知铁锈蚀与____有关。
(3)实验三:从长颈漏斗注入过氧化氢溶液,乙中发生反应的化学方程式为______。白磷的着火点为40 ℃。甲、丙中不同的现象是____。



 B.
B.  C.
C.  D.
D. 
 鸡蛋 B.
鸡蛋 B.  油条
油条 米粥 D.
米粥 D.  泡菜
泡菜

