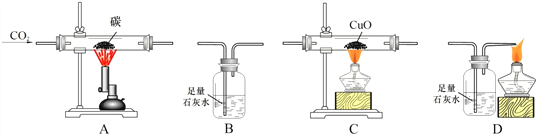
题目内容
【题目】关于下面两组对比实验的说法正确的是
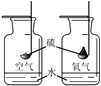
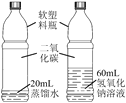
①对比硫在空气和氧气中燃烧的剧烈程度 | ②探究二氧化碳能否与氢氧化钠反应 |
|
|
A. 两个实验方案设计均合理 B. 实验①中可观察到硫在空气中燃烧 发出明亮的蓝紫色火焰
C. 实验②中右瓶变瘪的程度更大 D. 实验②反应后向右瓶中加入足量稀盐酸,可观察到冒气泡
【答案】C
【解析】A、进行对比试验时,实验②中的水和氢氧化钠溶液体积应该相等,故不正确;
B、实验①中可观察到硫在空气中燃烧发出淡蓝色火焰,故不正确;
C、实验②中右瓶变瘪的程度更大,这是因为二氧化碳能和氢氧化钠反应生成碳酸钠和水,而二氧化碳在水中的溶解度不大,故正确;
D、实验②中右瓶中的碳酸钠能和稀盐酸反应生成二氧化碳气体,能够观察到产生气泡,故不正确。

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目