题目内容
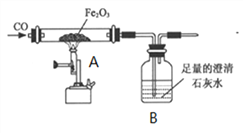
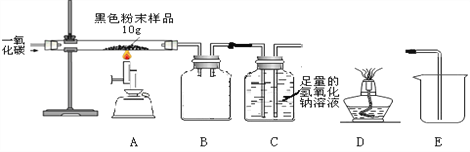
【题目】由铁,氧元素组成的固体5.8 g, 用足量的CO 还原,生成的气体全部被足量的澄清石灰水吸收,得到沉淀10g,则这种固体可能是
A. FeO B. Fe2O3与Fe的混合物
C. FeO与Fe3O4的混合物 D. Fe3O4
【答案】BD
【解析】设二氧化碳质量为![]() ,
,
![]()
44 100
![]() 10g
10g
![]()
![]() =4.4g,
=4.4g,
4.4g二氧化碳中氧元素质量为:4.4g×![]() ,
,
氧化亚铁、氧化铁、四氧化三铁和一氧化碳反应的化学方程式为: ![]()
![]()
![]() ,
, ![]()
![]()
![]() ,
, ![]()
![]()
![]() ,由反应的化学方程式可知,反应生成的二氧化碳中的氧元素一半来自于一氧化碳,一半来自于铁的氧化物,因此铁的氧化物中氧元素质量为:3.2÷2=1.6g,5.8g某种铁的氧化物中氧元素质量分数为:
,由反应的化学方程式可知,反应生成的二氧化碳中的氧元素一半来自于一氧化碳,一半来自于铁的氧化物,因此铁的氧化物中氧元素质量为:3.2÷2=1.6g,5.8g某种铁的氧化物中氧元素质量分数为: ![]() ,氧化亚铁、氧化铁、四氧化三铁中氧元素质量分数分别是:
,氧化亚铁、氧化铁、四氧化三铁中氧元素质量分数分别是: ![]() ,
, ![]() ,
, ![]() ,由以上计算可知,这种铁的氧化物可能是Fe2O3与Fe的混合物与Fe3O4。故选BD。
,由以上计算可知,这种铁的氧化物可能是Fe2O3与Fe的混合物与Fe3O4。故选BD。

练习册系列答案
相关题目