题目内容
【题目】请根据下图实验装置图回答问题:
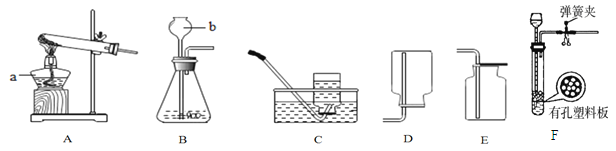
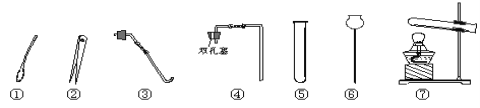
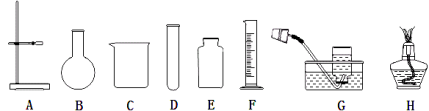
(1)写出仪器a,b的名称:a是 ,b是 .
(2)用A装置制取氧气的化学方程式是 ,可选用的收集装置是 (填序号).
(3)实验室用B、E装置制取CO2的化学方程式为 ,请写出用澄清石灰水检验二氧化碳时发生反应的化学方程式: 。若将发生装置由B改为F,其优点是 。
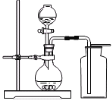
(4)将一瓶二氧化碳气体正立于烧杯中(装置见下图),敞口一会儿,集气瓶外壁上湿润的蓝色石蕊试纸自上面而下变红色,该现象说明分子具有 的性质,还说明二氧化碳气体 .
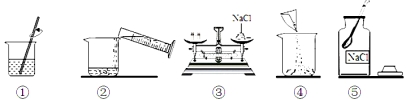
(5)某化学兴趣小组为了粗略测定一批石灰石样品中CaCO3的质量分数,设计并进行如下实验。实验装置如图所示,称取研细的2.60g石灰石样品,分4次加入稀盐酸,充分反应至不再产生气体为止。测得反应前后的有关质量如表:
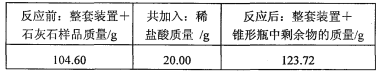
①计算石灰石样品中CaCO3的质量分数。
②若在上述实验过程中石灰石样品和所加酸液均无抛洒,根据图中装置判断,该实验结果可能 (填“偏大”、“偏小”或“准确”),原因是 。
【答案】
(1)酒精灯 长颈漏斗
(2)2KMnO4![]() K2MnO4 + MnO2 + O2↑ C或E
K2MnO4 + MnO2 + O2↑ C或E
(3)CaCO3 + 2HCl![]() CaCl2 + H2O + CO2↑ CO2 + Ca(OH)2
CaCl2 + H2O + CO2↑ CO2 + Ca(OH)2![]() CaCO3↓+ H2O
CaCO3↓+ H2O
随开随用、随关随停
(4)不断运动,密度比空气大
(5)76.9% 偏小,有一部分二氧化碳溶解在水中
【解析】
试题分析:(2)A装置属固固加热型,故可用高锰酸钾或氯酸钾制取氧气,加热高锰酸钾分解制取氧气的同时,还生成了锰酸钾和二氧化锰:2KMnO4![]() K2MnO4 + MnO2 + O2↑;氧气的密度比空气大,难溶于水,故可用向上排空气法或排水法收集,选C或E装置;
K2MnO4 + MnO2 + O2↑;氧气的密度比空气大,难溶于水,故可用向上排空气法或排水法收集,选C或E装置;
(3)B属固液在常温下反应是杂质,E装置是用向上排空气法收集,实验室一般用石灰石和稀盐酸反应制取二氧化碳气体:CaCO3 + 2HCl![]() CaCl2 + H2O + CO2↑;二氧化碳能使澄清的石灰水变浑浊,生成的是碳酸钙沉淀和水,反应的化学方程式为:CO2 + Ca(OH)2
CaCl2 + H2O + CO2↑;二氧化碳能使澄清的石灰水变浑浊,生成的是碳酸钙沉淀和水,反应的化学方程式为:CO2 + Ca(OH)2![]() CaCO3↓+ H2O;根据题意,石灰石接触到二稀盐酸后,反应便立即开始,不能人为控制反应的发生和停止,故可将石灰水放在隔板上,当需要反应停止时,关闭弹簧夹,固体和液体分离,可起到随开随用、随关随停的目的;
CaCO3↓+ H2O;根据题意,石灰石接触到二稀盐酸后,反应便立即开始,不能人为控制反应的发生和停止,故可将石灰水放在隔板上,当需要反应停止时,关闭弹簧夹,固体和液体分离,可起到随开随用、随关随停的目的;
(4)将一瓶二氧化碳气体正立于烧杯中(装置见右图),敞口一会儿,集气瓶外壁上湿润的蓝色石蕊试纸自上面而下变红色,该现象说明分子在不断的运动,二氧化碳的密度比空气大;
(5)依据质量守恒定律化学反应前后物质的总质量不变,那么减少的质量即为生成的二氧化碳的质量,故生成的二氧化碳的质量=104.60g+20g-123.72g=0.88g,根据二氧化碳的质量即可计算出碳酸钙的质量,
设碳酸钙的质量为x,那么:
CaCO3+2HCl==CaCl2+H2O+CO2↑
100 44
X 0.88g
100/x =44/0.88g
X=2g
石灰石样品中CaCO3的质量分数=2g/2.6g ×100% =76.9%
由于二氧化碳易溶液水,故实际测定的二氧化碳的质量偏小。
答:略