题目内容
【题目】向133.4克稀盐酸中加入锌粉(仅含不溶于酸的杂质),所加锌粉的质量与产生气体的质量的关系如下图所示。求:
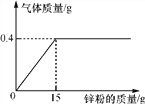
(1)此过程产生气体的最大质量是________g;
(2)原稀盐酸中溶质的质量分数为_____________________?(请写出计算过程)
【答案】 0.4 设原稀盐酸中溶质的质量分数为x。
Zn+2HCl===ZnCl2+H2↑
73 2
133.4 g×x 0.4 g
![]() =
=![]() x=10.9%答:原稀盐酸中溶质的质量分数为10.9%。
x=10.9%答:原稀盐酸中溶质的质量分数为10.9%。
【解析】由题中信息知,(1)此过程产生气体的最大质量是0.4g;
(2)解∶设原稀盐酸中溶质的质量分数为x
Zn+2HCl=ZnCl2+H2↑
73 2
l33.4g×x 0.4g
![]() =
=![]() ,x=10.9%。
,x=10.9%。
答∶(1)此过程产生气体的最大质量是0.4 g;(2)原稀盐酸中溶质的质量分数为10.9%。

练习册系列答案
相关题目