题目内容
【题目】现有甲、乙两份质量相等的氯酸钾,向甲中加入适量的二氧化锰,对两份加热至不再产生气体,下列图象正确的是( )
A.  B.
B. 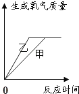 C.
C. 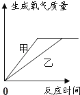 D.
D. 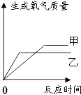
【答案】C
【解析】
催化剂只能加快化学反应速率,根据氯酸钾制取氧气的特点,不加催化剂时产生氧气的速率慢,加入催化剂后速率加快,甲加了二氧化锰,乙没有加,所以甲的反应速率快;氯酸钾的质量相同,甲与乙产生的氧气质量相等。
A、催化剂只能加快化学反应速率,不能改变生成物的质量,两份加热至不再产生气体时,生成的氧气擀质量应相等,与图像不符,故A错误;B、不加催化剂时产生氧气的速率慢,加入催化剂后速率加快,甲加了二氧化锰,乙没有加,甲的反应速率快,与图像不符,故B错误;C、不加催化剂时产生氧气的速率慢,加入催化剂后速率加快,甲加了二氧化锰,乙没有加,甲的反应速率快,催化剂只能加快化学反应速率,不能改变生成物的质量,两份加热至不再产生气体时,生的氧气应相等,与图像相符,故C正确;D、催化剂只能加快化学反应速率,不能改变生成物的质量,两份加热至不再产生气体时,生的氧气应相等,与图像不符,故D错误。故选C。

 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案【题目】空气中氧气含量测定的再认识。
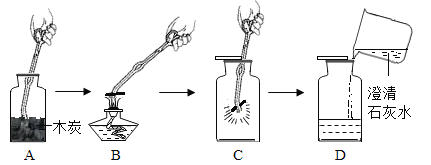
某化学兴趣小组的同学,在实验室用红磷、镁条、木炭等物质代替汞对空气中氧气的含量测定进行模拟探究。
实验一:A组同学通过燃烧红磷法测定空气中氧气的含量,装置如图所示,写出红磷燃烧的文字表达式___________________________

实验过程如下:
(1)用弹簧夹夹紧橡皮管;
(2)点燃燃烧匙内的红磷,观察到红磷燃烧,立即伸入瓶中并塞紧瓶塞.
(3)等装置冷却至室温后,打开弹簧夹。
(4)观察并记录水面的变化情况发现,集气瓶内上升的水面小于瓶内原有空气体积的五分之一,可能的原因是:___________
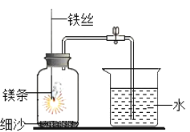
实验二:B组同学利用镁条在空气中燃烧测定空气中氧气含量,如图二所示,实验结束后,待装置冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%。根据空气的组成推测可能的原因是___________。
实验三:C组“利用木炭燃烧测定空气中氧气的体积分数”如图,根据经验,利用上图装置测定空气中氧气含量时,能否用木炭替代?___________(填“能”或“不能”)原因是:___________
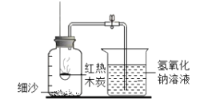
(提供资料)氢氧化钠能与二氧化碳反应生成碳酸钠和水,写出文字表达式___________该小组同学选择用氢氧化钠溶液吸收生成的二氧化碳气体,但进入集气瓶中水的体积分数仍然小于1/5 。
(提出问题)是什么原因导致测量不准确呢?
(猜想与假设)他们分别作了如下猜想:
甲同学:可能是木炭取的量过少;
乙同学:可能是木炭燃烧没有消耗完集气瓶中的氧气;
丙同学:可能是木炭与空气反应生成了其他气体。
(查阅资料)
资料一:木炭、棉花和蜡烛在密闭容器内燃烧停止后,残留氧气的体积分数分别高达14.0%,8.0%和16.0%。
资料二:木炭在密闭容器中不充分燃烧会生成一氧化碳气体。
资料三:一氧化碳能与灼热的氧化铜粉末(黑色)反应生成铜(红色)和二氧化碳气体
(探究一)
小组同学发现实验结束后,燃烧匙中还有残留的黑色固体,可知____同学的猜想不合理。
(探究二)乙同学又利用上述装置设计了如下实验,请你填写下表:
实验步骤 | 实验现象 | 实验结论 |
将足量木炭点燃,迅速插入装有氧气的集气瓶中 | ___________ | 木炭燃烧没有消耗完集气瓶中的氧气 |
待装置冷却后,将燃着的___________(填“棉花”或蜡烛)再伸入集气瓶中 | ___________ |
(探究三)
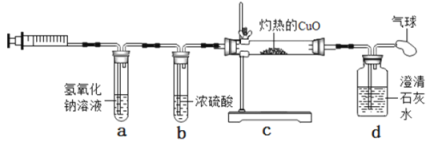
小明从木炭燃烧产物的角度猜想还可能是生成了______导致测量结果小于1/5;于是用注射器抽取集气瓶内的气体做了如图所示的实验,当观察到d中______________(填实验现象),可证明小明的猜想成立。
(经典对比)通过与上述实验对比,拉瓦锡选择用汞的优点有___________

A.能将密闭装置内空气中的氧气几乎耗尽
B.在汞槽中起到液封作用
C.实验过程中没有污染
D.生成的化合物加热分解又能得到汞和氧气
【题目】某课外活动小组就催化剂对化学反应速率的影响进行了有关探究,已知二氧化锰可作为过氧化氢分解产生氧气的催化剂。同学在用过氧化氢溶液与二氧化锰制取氧气的过程中,发现反应的速率慢,产生的气泡少。为此,他们进行了如下探究:
(猜想与假设)
①分解速度慢可能与过氧化氢溶液的浓度有关。
②分解速度慢可能与二氧化锰的质量有关。
(进行实验)根据图甲进行如下实验。
实验1:用26mg 二氧化锰与5mL不同浓度的过氧化氢溶液进行实验,压强变化如乙图1。
实验2:用5mL 1.5%过氧化氢溶液与不同质量的二氧化锰进行实验,压强变化如乙图2。
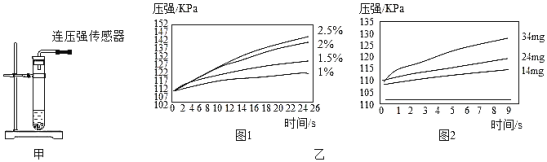
(解释与结论)
(1)过氧化氢溶液制取氧气的文字表达式为__________________。
(2)实验1得到的结论是过氧化氢溶液的浓度越_____________,分解速度越快。实验2得到的结论是二氧化锰的质量越_______________,分解速度越慢。
(3)小组同学通过查阅资料得知:同一个反应的催化剂可能有多种。
(查阅资料)除二氧化锰外,氧化铜、氧化铁也可以作为氯酸钾分解的催化剂。
(进行实验)取等质量的氯酸钾按下表进行实验:测定氯酸钾分解产生氧气的温度。
实验编号 | 实验药品 | 分解温度 |
氯酸钾 | 580 | |
氯酸钾、二氧化锰(质量比1:1) | 350 | |
氯酸钾、氧化铜(质量比1:1) | 370 | |
氯酸钾、氧化铁(质量比1:1) | 390 |
(分析数据、得出结论)
(1)由实验______与实验![]() 对比,证明氧化铁可作为氯酸钾分解的催化剂。
对比,证明氧化铁可作为氯酸钾分解的催化剂。
(2)实验所用的三种物质中,催化效果最好的是______________。
(反思)证明氧化铜是该反应的催化剂,还要验证它在化学反应前后的质量和____没有改变。