题目内容
【题目】硼在自然界中的含量相当丰富,主要以硼酸和硼酸盐的形式存在。硼可形成 H3BO3、B2O3、NaBO2等化合物,用途广泛。天然产的硼砂(NaBO·10HO),在中国古代就已作为药物,叫做蓬砂或盆砂。
(1)硼酸可由硼砂(NaBO·10HO)与盐酸加热反应制得。该反应的化学方程式为
NaBO·10HO + 2HCl![]() 4H3BO3 + 2X+ 5H2O,则X的化学式为____________
4H3BO3 + 2X+ 5H2O,则X的化学式为____________
(2)NaBO中硼元素的化合价为_____,从物质分类的角度看,NaBO属于_____(填选项)
A. 化合物 B.氧化物 C.酸 D.盐
(3)硼在高温下能与一些单质发生反应,如能在空气中燃烧生成BO和少量BN,该反应的化学方程式为:____________。
(4)B还能从许多稳定的氧化物中夺取氧,可知B具有_________性。
【答案】NaCl 。+3,A、DN2 +6B +3O2![]() 2B2O3 +2BN 。还原。
2B2O3 +2BN 。还原。
【解析】
(1)根据质量守恒定律,反应前后原子个数不变,故X的化学式为NaCl;
(2)NaBO中钠元素化合价为+1,氧元素化合价为-2,根据化合物中元素正负化合价代数和为零,可知硼元素化合价为+3;NaBO中含有三种元素,属于纯净物中的化合物,同时该化合物由金属离子和酸根离子构成,也属于盐类,故选AD;
(3)硼能在空气中燃烧生成BO和少量BN,根据生成物的元素组成和质量守恒定律可知,反应物为硼、氧气和氮气,故反应化学方程式为N2 +6B +3O2![]() 2B2O3 +2BN;
2B2O3 +2BN;
(4)在化学反应中,能从氧化物中夺取氧的物质具有还原性,故B具有还原性。

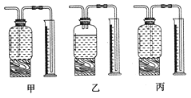
【题目】小明、小强和小峰在学习了“质量守恒定律”后来到化学实验室亲自进行了实验探究,如图是他们分别设计的实验,请你与他们一起进行探究,并回答问题.

实验1:称量镁条,点燃,待反应结束后,再称量.
实验2:将盛有稀盐酸的小试管放入盛有锌粒的烧杯中称量,然后使稀盐酸与锌粒接触,充分反应后再称量.
实验3:将盛有氢氧化钠溶液的小试管放入盛有硫酸铜溶液的锥形瓶中称量,然后使氢氧化钠溶液与硫酸铜溶液混合,充分反应后再称量.
数据见下表:(锌与盐酸反应:Zn+2HCl=ZnCl2+H2↑;氢氧化钠溶液与硫酸铜溶液反应:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4)
编号 | 实验1 | 实验2 | 实验3 |
反应前称量质量 | 9.6g | 212.6g | 118.4g |
反应后称量质量 | 16.0g | 212.4g | 118.4g |
(1)写出实验1反应的化学方程式_____.
(2)上述三个反应_____(填“符合”或“不符合”)质量守恒定律,实验_____正确反映了反应物与生成物的质量关系.
(3)由上述实验我们得到启示,探究_____的反应验证质量守恒定律,实验必须在密闭的装置中进行.
(4)由质量守恒定律可知,化学反应前后,一定不变的是_____(填序号).
①物质种类②元素种类③原子种类④分子种类⑤分子数目⑥原子数目.
【题目】曾有一段时间在微信上流传了一种懒人火锅。这种火锅分上下两层,食用前只需要把带底料的食材放入上层,然后将加热包放入下层,并加入一定量冷水,立即就能产生热量给上层的食材加热,使汤料沸腾,并保温1到2个小时。某化学兴趣小组对这种懒人火锅的原理及使用后加热包中的成分进行了研究。

(查阅资料)发热包的主要成分是:碳酸钠、焙烧硅藻土(难溶于水)、铁粉、焦炭粉、活性炭、氯化钠、生石灰。
(实验探究)
(1)同学甲经过对发热包成分的研究后,认为发热主要原理是________(用化学方程式表示)
(2)同学乙从已经使用完的发热包中取少量固体混合物于烧杯中,缓慢加入足量蒸馏水,边加边搅拌,静置,过滤得滤液。
(3)同学丙在上述实验的基础上,对滤液中所含阴离子的种类进行探究,请帮她完成实验过程。提供的试剂:稀盐酸、稀硝酸、酚酞、AgNO3溶液、Ba(NO3)2溶液、Mg(NO3)2溶液
实验操作 | 预期现象 | 结论 |
步骤1:取少量滤液于试管中,加入_______。 | _______ | 滤液中没有CO32- |
步骤2:另取少量滤液于试管中,加入过量_____。 | _________ | 滤液中含有OH- |
步骤3:_________ | 产生白色沉淀 | 滤液中含有______ |