某化学兴趣小组在用铜丝和银丝做实验时,发现久置的铜丝表面能生成绿色的铜锈,兴趣小组对铜生锈的条件进行了以下探究。
(查阅资料)铜锈的主要成分为Cu2(OH)2CO3。
(作出猜想)铜生锈可能与空气中的氧气有关外,还可能与_____有关,作出此猜想的依据是_____。
(实验设计)兴趣小组同学取4根铜丝设计了如下图所示的四个实验。
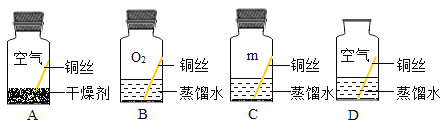
他们为了除去铜丝表面的污物,实验前应该做的操作是_____。C瓶中的m应该是_____。
(现象分析)若干天后,发现只有D瓶中的铜丝表面出现绿色的铜锈,其他瓶中的铜丝表面均无铜锈出现。
(1)实验B、C瓶中所使用的蒸馏水是经煮沸后迅速冷却的蒸馏水,其目的是_____。
(2)通过B瓶与D瓶中的现象对比,可以得出铜生锈与_____有关的结论。
(实验结论)由上述四个实验可以分析得出猜想成立,写出铜生锈的化学方程式_____。
(讨论交流)在同样环境下银丝依旧光亮如新,原因是_____。
 测定pH B.
测定pH B. 检查装置气密性
检查装置气密性 验满CO2 D.
验满CO2 D. 称量食盐
称量食盐 测定pH B.
测定pH B. 检查装置气密性
检查装置气密性 验满CO2 D.
验满CO2 D. 称量食盐
称量食盐