题目内容
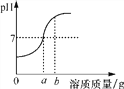
【题目】用稀硫酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的pH变化如图所示。
(1)写出该反应的化学方程式________________________。
(2)该实验是将____________(填“稀硫酸”或“氢氧化钠溶液”)滴加到另一种溶液中。
(3)当所加溶液中溶质的质量为b g时,所得溶液中的溶质为____________(写化学式)。
(4)完全中和一定量的某硫酸溶液,需要100 g 8%的NaOH溶液,若改用100 g 8%的KOH溶液,则反应后溶液的pH________(填“>”“<”或“=”)7。
【答案】 2NaOH+H2SO4===Na2SO4+2H2O 氢氧化钠溶液 Na2SO4、NaOH <
【解析】试题分析∶(1)化学方程式2NaOH+ H2SO4=Na2SO4+2H2O(2)首先PH<7,应将NaOH滴加到稀硫酸中。(3)此时氢氧化钠过量,所得溶液中的溶质为Na2SO4、NaOH (4)氢氧化钾质量少,溶液呈酸性。PH<7

练习册系列答案
相关题目