题目内容
【题目】图中A、B、C、D、E、F分别是表示六种物质,B、C、D、F分别属于酸、碱、盐、氧化物四种类别的一种,A是目前世界年产量最高的金属,B是可溶性银盐,D与E发生的反应属于中和反应.(图中用“﹣”或“⌒”表示两种物质之间能发生化学反应,用“→”或“ ![]() ”表示一种物质可以转化为另一种物质,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行).请回答下列问题:
”表示一种物质可以转化为另一种物质,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行).请回答下列问题: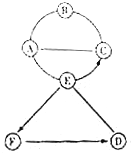
(1)分别写出B、C、E、F物质的化学式(或溶质的化学式).
B: C: E: F:
(2)写出A与B发生反应的化学方程式;
(3)写出B与C发生反应的实验现象 .
【答案】
(1)AgNO3;CuCl2;HCl;H2O
(2)Fe+2AgNO3=Fe(NO3)2+2Ag
(3)有白色沉淀生成
【解析】(1)B、C、D、F分别属于酸、碱、盐、氧化物四种类别的一种,A是目前世界年产量最高的金属,所以A是铁,B是可溶性银盐,所以B是硝酸银,D与E发生的反应属于中和反应,A会与E反应,所以E可以是盐酸,E会转化成F,F会转化成D,D是碱,所以D是氢氧化钙,F是水,盐酸转化成的C会与硝酸银、铁反应,所以C是氯化铜,经过验证,推导正确,所以B是AgNO3 , C是CuCl2 , E是HCl,F是H2O;(2)A与B发生的反应是铁和硝酸银反应生成硝酸亚铁和银,化学方程式为:Fe+2AgNO3=Fe(NO3)2+2Ag;(3)B与C发生的反应是硝酸银和氯化铜反应生成氯化银沉淀和硝酸铜,所以实验现象为:有白色沉淀生成.
所以答案是:(1)AgNO3 , CuCl2 , HCl,H2O;(2)Fe+2AgNO3=Fe(NO3)2+2Ag;(3)有白色沉淀生成.
【考点精析】掌握书写化学方程式、文字表达式、电离方程式是解答本题的根本,需要知道注意:a、配平 b、条件 c、箭号.

【题目】分类、类比是学习化学常用的方法.
(1)化学实验可按其主要目的分为:探究物质的性质、混合物的分离提纯,探究物质的含量等.因此应将下列实验中的B与(填“A”或“C”或“D”)归为一类,依据是 .
|
|
|
|
A | B | C | D |
(2)再反应C+CO2![]() 2CO中,具有氧化性的反应物是 . 请写出一个两种化合物发生反应的化学方程式(其中一种化合物体现氧化性,另一种化合物体现还原性) .
2CO中,具有氧化性的反应物是 . 请写出一个两种化合物发生反应的化学方程式(其中一种化合物体现氧化性,另一种化合物体现还原性) .