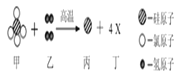
题目内容
【题目】下面是实验室常用制取气体的装置图,根据装置图回答下列问题
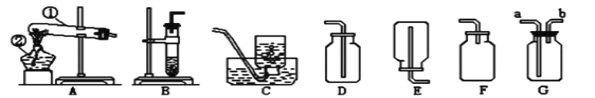
(1)写出标有①②序号的仪器的名称:①______________,②_____________
(2)实验室在B装置中用双氧水与二氧化锰混合制取氧气的化学方程式_______________________
(3)实验室制取二氧化碳的化学方程式:_______________________。若用G装置收集二氧化碳,空气会从_______管口排出。
(4)硫化氢(H2S)在通常状况下是一种无色、有臭鸡蛋气味的气体,密度比空气大,极易溶于水,其水溶液称为氢硫酸。实验室常用硫化亚铁和稀硫酸反应来制取硫化氢气体,其反应的化学方程式为:FeS+H2S04=FeS04+H2S↑,则实验室制取硫化氢的发生装置可选_____________________装置,收集硫化氢可选用_______________装置,干燥硫化氢可选用下列的_______(填字母)。
A.无水氯化钙 B.碱石灰
【答案】 试管 酒精灯 2H2O2![]() 2H2O +O2↑ CaCO3 +2HCl === CaCl2 +H2O +CO2↑ b B D A
2H2O +O2↑ CaCO3 +2HCl === CaCl2 +H2O +CO2↑ b B D A
【解析】本考点主要考查了仪器的名称、气体的干燥、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强。气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关。
(1)标有①②序号的仪器的名称分别为:试管 酒精灯
(2)过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,化学方程式是:2H2O2![]() 2H2O +O2↑;
2H2O +O2↑;
(3)实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,化学方程式是CaCO3 +2HCl === CaCl2 +H2O +CO2↑;二氧化碳的密度比空气的密度大。若用G装置收集二氧化碳,二氧化碳从a管口进入,空气会从b管口排出;
(4)实验室常用硫化亚铁和稀硫酸反应来制取氨气,不需要加热,选用的发生装置是B;硫化氢气体的密度比空气大,极易溶于水,因此只能用向上排空气法收集,收集装置选用D;碱石灰能与硫化氢反应,无水氯化钙不能与硫化氢反应,硫化氢气体可以用无水氯化钙干燥。故选A。

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
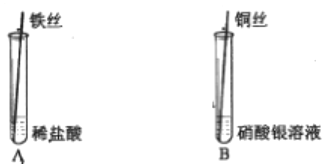
步步高口算题卡系列答案【题目】学习酸碱盐知识后,同学们知道碳酸钠溶液与氢氧化钙溶液能发生反应,可观察到溶液变浑浊。甲组同学进行右图所示的实验,却未观察到预期现象。

【提出问题】未观察到浑浊的原因是什么?
【猜想和假设】
①与氢氧化钙溶液的浓度有关。若使用更大浓度的氢氧化钙溶液,会迅速产生浑浊。
②与碳酸钠溶液的浓度有关。若使用更大浓度的碳酸钠溶液,会迅速产生浑浊。经讨论,同学们认为猜想①不合理,其理由是 。
【进行实验】乙组同学针对猜想②进行实验。
实验目的 | 实验操作 | 实验现象 | |
探究猜想② | 取4支试管,向其中分别加入 | 碳酸钠溶液浓度/% | 是否浑浊 |
10 | 不浑浊 | ||
5 | 不浑浊 | ||
1 | 浑浊 | ||
0.5 | 浑浊 | ||
【解释与结论】
(1)补全上述实验操作:取4支试管,向其中分别加入 。
(2)氢氧化钙溶液与碳酸钠溶液混合出现浑浊的化学方程式是 。
(3)乙组实验证明:猜想②不成立,碳酸钠溶液浓度在0.5~10%的范围内,能否出现浑浊与碳酸钠溶液的浓度有关,其关系是 。
【实验反思】
(1)丙组同学对乙组所做实验中未出现浑浊的原因进行探究。设计了多组实验,其中部分同学的实验过程及结果如下:

丙组同学的实验目的是 。
(2)依据乙、丙两组的实验探究,丁组同学仍使用甲组的仪器和药品对甲组实验进行了改进,当滴入几滴某溶液后,溶液迅速变浑浊。其实验操作是 。