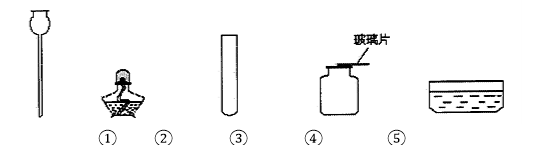
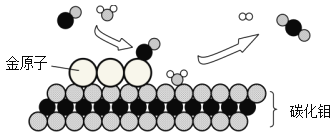
题目内容
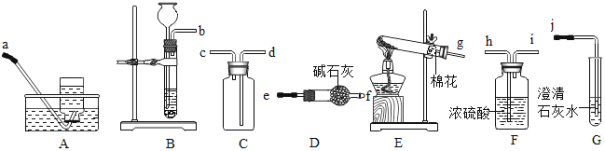
【题目】如图是实验室中常见装置,回答下列问题。
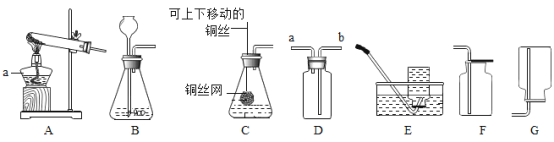
(1)A中仪器a的名称是___________________。
(2)若用B装置作为实验室制取氧气的发生装置,反应的化学方程式是______________,若用F装置收集,验满的方法是_____________。
(3)实验室可用C装置作为发生装置制备二氧化碳,该装置的主要优点是________________。向集满CO2的集气瓶中加入澄清石灰水,反应的化学方程式为__________。
(4)实验室里通常用MnO2与浓盐酸在加热条件下制取氯气,同时生成MnCl2和水,请写出该反应的化学方程式___________,如果用D装置收集氯气( Cl2的相对分子质量为71),气体应从_____________(填“a”或“b”)端管口通人。
【答案】酒精灯 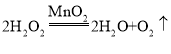 把带火星的木条放在集气瓶口,若木条复燃则集满 能够控制反应的发生与停止
把带火星的木条放在集气瓶口,若木条复燃则集满 能够控制反应的发生与停止 ![]()
![]() b
b
【解析】
(1)A中仪器a的名称是酒精灯,用于加热。
(2)装置B为固液常温型制取氧气,故化学方程式为 ,F装置是用向上排空气法收集氧气,氧气具有助燃性,故验满氧气的方法为把带火星的木条放在集气瓶口,若木条复燃则集满。
,F装置是用向上排空气法收集氧气,氧气具有助燃性,故验满氧气的方法为把带火星的木条放在集气瓶口,若木条复燃则集满。
(3) C装置是使用可以抽动的铜丝,其优点可以通过抽动铜丝控制大理石与稀盐酸的接触与分离,从而控制反应的发生与停止。向集满CO2的集气瓶中加入澄清石灰水,澄清石灰水的主要成分为Ca(OH)2,则![]() 。
。
(4)已知反应物为MnO2与浓盐酸,条件为加热,产物为氯气、MnCl2和水,故化学方程式为![]() ;氯气的相对分子质量大于29,即密度大于空气,收集氯气应该从b端进入。
;氯气的相对分子质量大于29,即密度大于空气,收集氯气应该从b端进入。

 巧学巧练系列答案
巧学巧练系列答案【题目】小滨同学为了测定某珍珠粉中钙元素的质量分数,称取12.5g珍珠粉样品,进行四次高温煅烧、冷却、称量剩余固体的重复操作(杂质不参加反应),记录数据如下:
操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量/g | 10.8 | 9.6 | 8.1 | 8.1 |
(1)完全反应后生成二氧化碳的质量为________________________ g。
(2)求该珍珠粉中碳酸钙的质量分数___________________。
(3)求该珍珠粉中钙元素的质量分数___________________。