题目内容
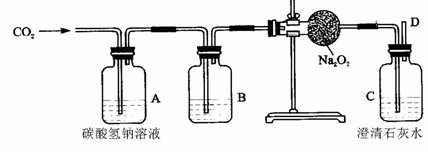
27.(11分)“嫦娥一号”飞船的成功发射是我国航天事业的又一里程碑。金属过氧化物等可作宇宙飞船或潜水艇中的氧气再生剂,如:过氧化钠(Na2O2)在常温下能与人呼出的二氧化碳反应生成氧气,化学方程式为:2Na2O2+2CO2===2Na2CO3+O2;(过氧化钠还能与盐酸、水等物质发生反应产生氧气)为了验证该反应中氧气的产生,某兴趣小组的同学设计了如右图所示的实验。
(1)实验室确定气体发生装置时应考虑的因素是 ;
制取CO2的装置,应从下列图1、图2、图3中选择 。
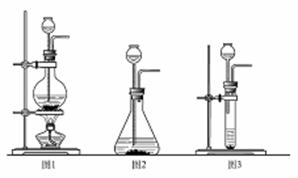
(2)检查图2装置的气密性的方法是:将装置中导气管上的胶皮管用弹簧夹夹住,往长颈漏斗中注入水至液面高出漏斗颈的下端管口,若能观察到 现象,即可证明装置不漏气。
(3)设计A、B装置的目的是净化导入的纯净且干燥的CO2 。其中,①A装置的具体功能是________________所发生的化学方程式是 ;
②B装置的具体功能是 ,其瓶内液体应是___________ ;
(4)为了确定CO2跟Na2O2反应产生的气体是氧气,最后还要采用的验证实验操作是____________________________________________________________________。
(5)表明二氧化碳没有被过氧化钠完全吸收的现象是 。
(6)常温下水也能与Na2O2反应,生成氧气和氢氧化钠,写出该反应的化学方程式。
;
(7)某潜水艇上有4人,如果每人每小时消耗的氧气在某温度和压强条件下体积为50L,则该潜水艇中每天需要过氧化钠多少千克?(已知:在上述温度和压强条件下氧气的密度为1.5g/L) 。
(11分)
(1) 反应物的状态和反应条件等 图2
(2) 漏斗颈中形成一段稳定的水柱(或液面不再下降)等
(3) ①吸收二氧化碳中混有的氯化氢气体 NaHCO3+HCl==NaCl+H2O+CO2↑
②干燥二氧化碳 浓硫酸
(4)将带火星的木条放在集气瓶上方的导管口附近
(5)C装置处的澄清石灰水变浑浊
(6)2Na2O2+2H2O===4NaOH+O2↑
(7)35.1kg。


 D.原子结构示意图为
D.原子结构示意图为