题目内容
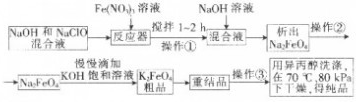
高铁酸钾是一种高效的多功能水处理剂,具有氧化、吸附、絮凝、助凝、杀菌、除臭等作用,高铁酸钾的开发和利用正日益显示出其广阔的应用前景.其制备路线如下:
试回答下列问题
(1)操作①搅拌的目的是 .
(2)操作②与操作③相同,该操作的名称是
(3)慢慢滴加KOH饱和溶液发生的复分解反应的化学方程式为 .
(4)高铁酸钾作为净水剂对人的身体还有一个的好处是补铁,K2FeO4中铁元素的化合价为 价
(5)操作③后剩余的母液中,可循环使用的物质的化学式是 .
【答案】分析:(1)根据玻璃棒搅拌的作用分析
(2)根据分离混合物的方法分析
(3)根据复分解反应的特点及化学方程式的书写原则书写方程式
(4)根据化合物中正负化合价的代数和为0分析
(5)根据重结晶后母液中的溶质分析
解答:解:(1)氢氧化钠和NaClO的混合液中加入硝酸亚换溶液发生化学反应,为使其充分反应可用玻璃棒搅拌.
(2)操作②与操作③都是将固体从液体中分离出来,因此可采用过滤
(3)慢慢滴加KOH饱和溶液后,氢氧化钾和高铁酸钠发生复分解反应生成高铁酸钾和氢氧化钠,化学方程式为 2KOH+Na2FeO4=K2FeO4+2NaOH.
(4)K2FeO4中钾元素+1价,氧元素-2价,根据正负化合价的代数和为0可知铁元素的化合价为+6价
(5)操作③后剩余的母液中还含有氢氧化钠溶液可循环使用.
故答案为:(1)使其充分反应.
(2)过滤
(3)2KOH+Na2FeO4=K2FeO4+2NaOH.
(4)+6
(5)NaOH
点评:本题结合高铁酸钾(K2FeO4)的制备主要考查了氧化还原反应的知识、离子的检验等,培养了学生运用知识的能力.
(2)根据分离混合物的方法分析
(3)根据复分解反应的特点及化学方程式的书写原则书写方程式
(4)根据化合物中正负化合价的代数和为0分析
(5)根据重结晶后母液中的溶质分析
解答:解:(1)氢氧化钠和NaClO的混合液中加入硝酸亚换溶液发生化学反应,为使其充分反应可用玻璃棒搅拌.
(2)操作②与操作③都是将固体从液体中分离出来,因此可采用过滤
(3)慢慢滴加KOH饱和溶液后,氢氧化钾和高铁酸钠发生复分解反应生成高铁酸钾和氢氧化钠,化学方程式为 2KOH+Na2FeO4=K2FeO4+2NaOH.
(4)K2FeO4中钾元素+1价,氧元素-2价,根据正负化合价的代数和为0可知铁元素的化合价为+6价
(5)操作③后剩余的母液中还含有氢氧化钠溶液可循环使用.
故答案为:(1)使其充分反应.
(2)过滤
(3)2KOH+Na2FeO4=K2FeO4+2NaOH.
(4)+6
(5)NaOH
点评:本题结合高铁酸钾(K2FeO4)的制备主要考查了氧化还原反应的知识、离子的检验等,培养了学生运用知识的能力.

练习册系列答案
相关题目
高铁酸钾(K2FeO4)是一种集氧化、吸附、杀菌、灭藻、脱色、除臭等为一的新型高效水处理剂.下列关于该物质的说法正确的是( )
| A、高铁酸钾是由2个钾原子、一个铁原子和4个氧原子构成的 | B、高铁酸钾是一种混合物 | C、高铁酸钾中含有两种金属元素 | D、高铁酸钾分子是由6个原子构成的 |