题目内容
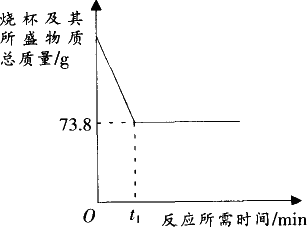
淄博市位于鲁中山地和华北平原的接壤处,具有丰富的石灰石矿产资源.南部山区某矿山的石灰石样品中含有二氧化硅杂质(二氧化硅是一种既不溶于水也不与盐酸反应且耐高温的固体).阳光学校的同学们想测定该样品中碳酸钙的质量分数,他们采取了一块石灰石样品,将其敲碎后,称出6 g放入烧杯内(烧杯质量为20 g).然后加入50 g某一定溶质质量分数的稀盐酸,用玻璃棒搅拌至不再产生气泡为止.反应所需时间(T)和烧杯及其所盛物质总质量(M)的关系如下图所示.试回答:
(1)将石灰石样品敲打粉碎的主要目的是________.
(2)实验结束时,共放出多少二氧化碳?
(3)该石灰石样品中碳酸钙的质量分数是多少?
答案:
解析:
解析:
|
(1)增大接触面积,加快反应速率 (2)由图可看出,在t1℃时,石灰石样品中的碳酸钙已完全反应,此时产生二氧化碳的质量为:20 g+6 g+50 g-73.8 g=2.2 g或76 g-73.8 g=2.2 g (3)设6 g石灰石样品中所含碳酸钙的质量为x,则 该石灰石样品中碳酸钙的质量分数是:5 g÷6 g×100%=83.3% |

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
