题目内容
现有如图所示仪器或装置,请回答下列问题:
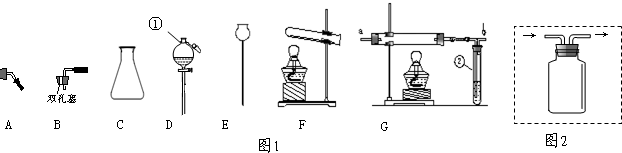
(1)写出图1中标有①、②仪器的名称:①______,②______.
(2)要检验G装置气密性方法是:在a处套上一个夹好铁夹的橡胶管,用酒精灯在玻璃管处微热,②中有______;冷却后在______,说明气密性良好.
(3)用高锰酸钾制取氧气时,发生装置应选______(填字母),选择的根据是______,化学方程式为______.
(4)实验室制取二氧化碳时,为了便于控制反应速率,发生装置可选用图1中的______(填字母),反应的化学方程式为______.检验该气体满瓶的方法是______.
用该装置还可以制取______气体,化学方程式为______.
(5)草酸(H2C2O4) 固体在浓硫酸作用下发生反应:H2C2O4  CO2↑+CO↑+X,
CO2↑+CO↑+X,
其中X的化学式是______;要除去其中的CO2可用右图装置,请将图2中的“导气管”补画完整,(图中“→”表示气体流向)
瓶中的试剂最好是______(填小写字母):
a.烧碱溶液 b.浓硫酸 c.澄清石灰水.
(6)若进行CO还原CuO的实验,可选择G装置,②中试剂的名称为______.尾气的处理方法是:______.
解:(1)标号仪器分别是分液漏斗、试管;
(2)要检验G装置气密性方法是:在a处套上一个夹好铁夹的橡胶管,用酒精灯在玻璃管处微热,若装置不漏气,温度升高,则②中有气泡产生,冷却后导管中上升一段水柱;
(3)用高锰酸钾制取氧气,属于固体加热型,故选发生装置F,反应的方程式是:2KMnO4 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(4)为了便于控制反应速率,可选分液漏斗,并选择双孔塞,作为反应容器的锥形瓶,大理石和稀盐酸反应生成氯化钙、水和二氧化碳,方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;检验二氧化碳是否收集满的方法是将燃着的木条放于集气瓶口,观察木条是否熄灭进行判断;用双氧水来制取氧气也可用此装置,反应方程式是:2H2O2 2H2O+O2↑;
2H2O+O2↑;
(5)据反应前后原子的种类和数目不变,由H2C2O4 CO2↑+CO↑+X,可知反应前氢原子2个,碳原子2个氧原子4个,生成物中碳原子2个,氧原子3个,所以X的化学式是H2O;洗气装置中导管要长进导出,便于将气体与氢氧化钠溶液更好的接触、反应掉;澄清石灰水中的溶质氢氧化钙是微溶于水,即便是饱和溶液里面含的氢氧化钙也很少,一般无法除净二氧化碳,而烧碱极易溶于水,水溶液中溶质含量大可应将二氧化碳处理干净;
CO2↑+CO↑+X,可知反应前氢原子2个,碳原子2个氧原子4个,生成物中碳原子2个,氧原子3个,所以X的化学式是H2O;洗气装置中导管要长进导出,便于将气体与氢氧化钠溶液更好的接触、反应掉;澄清石灰水中的溶质氢氧化钙是微溶于水,即便是饱和溶液里面含的氢氧化钙也很少,一般无法除净二氧化碳,而烧碱极易溶于水,水溶液中溶质含量大可应将二氧化碳处理干净;
(6)若进行CO还原CuO的实验,检验气体生成物用澄清的石灰水,处理一氧化碳尾气可用酒精灯点燃,利用其可燃性将其燃烧掉或用气球收集起来;
故答案为:(1)分液漏斗;试管;
(2)气泡冒出;导管中上升一段水柱;
(3)F;反应物是固体,反应条件是加热;2KMnO4 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(4)BCD;CaCO3+2HCl═CaCl2+H2O+CO2↑;将燃烧的木条放于集气瓶口,若木条熄灭则收集满了;氧气;2H2O2 2H2O+O2↑;
2H2O+O2↑;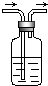
(5)H2O;如下图;a;
(6)澄清的石灰水;在试管口处放一酒精灯点燃(合理即可)
分析:(1)据常用仪器回答;
(2)据检查装置气密性的方法分析解答;
(3)据反应物状态和反应条件选择发生装置,据反应原理书写方程式;
(4)为了便于控制反应速率,可选分液漏斗,并选择双孔塞,作为反应容器的锥形瓶,并据反应原理书写方程式;检验二氧化碳是否收集满的方法是将燃着的木条放于集气瓶口,观察木条是否熄灭进行判断;固体和液体反应不需加热制取气体的装置,还可以用双氧水来制取氧气;
(5)据反应前后原子的种类和数目不变判断物质的化学式;洗气装置中导管要长进导出,澄清石灰水中的溶质氢氧化钙是微溶于水,即便是饱和溶液里面含的氢氧化钙也很少,一般无法除净二氧化碳,而烧碱极易溶于水,水溶液中溶质含量大可应将二氧化碳处理干净;
(6)若进行CO还原CuO的实验,检验气体生成物用澄清的石灰水,处理一氧化碳尾气可用酒精灯点燃,利用其可燃性将其燃烧掉.
点评:本题考查知识综合而全面,同学们要加强基础知识的积累,才能结合具体情景灵活分析解答问题.
(2)要检验G装置气密性方法是:在a处套上一个夹好铁夹的橡胶管,用酒精灯在玻璃管处微热,若装置不漏气,温度升高,则②中有气泡产生,冷却后导管中上升一段水柱;
(3)用高锰酸钾制取氧气,属于固体加热型,故选发生装置F,反应的方程式是:2KMnO4
 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;(4)为了便于控制反应速率,可选分液漏斗,并选择双孔塞,作为反应容器的锥形瓶,大理石和稀盐酸反应生成氯化钙、水和二氧化碳,方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;检验二氧化碳是否收集满的方法是将燃着的木条放于集气瓶口,观察木条是否熄灭进行判断;用双氧水来制取氧气也可用此装置,反应方程式是:2H2O2
 2H2O+O2↑;
2H2O+O2↑;(5)据反应前后原子的种类和数目不变,由H2C2O4
 CO2↑+CO↑+X,可知反应前氢原子2个,碳原子2个氧原子4个,生成物中碳原子2个,氧原子3个,所以X的化学式是H2O;洗气装置中导管要长进导出,便于将气体与氢氧化钠溶液更好的接触、反应掉;澄清石灰水中的溶质氢氧化钙是微溶于水,即便是饱和溶液里面含的氢氧化钙也很少,一般无法除净二氧化碳,而烧碱极易溶于水,水溶液中溶质含量大可应将二氧化碳处理干净;
CO2↑+CO↑+X,可知反应前氢原子2个,碳原子2个氧原子4个,生成物中碳原子2个,氧原子3个,所以X的化学式是H2O;洗气装置中导管要长进导出,便于将气体与氢氧化钠溶液更好的接触、反应掉;澄清石灰水中的溶质氢氧化钙是微溶于水,即便是饱和溶液里面含的氢氧化钙也很少,一般无法除净二氧化碳,而烧碱极易溶于水,水溶液中溶质含量大可应将二氧化碳处理干净;(6)若进行CO还原CuO的实验,检验气体生成物用澄清的石灰水,处理一氧化碳尾气可用酒精灯点燃,利用其可燃性将其燃烧掉或用气球收集起来;
故答案为:(1)分液漏斗;试管;
(2)气泡冒出;导管中上升一段水柱;
(3)F;反应物是固体,反应条件是加热;2KMnO4
 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;(4)BCD;CaCO3+2HCl═CaCl2+H2O+CO2↑;将燃烧的木条放于集气瓶口,若木条熄灭则收集满了;氧气;2H2O2
 2H2O+O2↑;
2H2O+O2↑;
(5)H2O;如下图;a;
(6)澄清的石灰水;在试管口处放一酒精灯点燃(合理即可)
分析:(1)据常用仪器回答;
(2)据检查装置气密性的方法分析解答;
(3)据反应物状态和反应条件选择发生装置,据反应原理书写方程式;
(4)为了便于控制反应速率,可选分液漏斗,并选择双孔塞,作为反应容器的锥形瓶,并据反应原理书写方程式;检验二氧化碳是否收集满的方法是将燃着的木条放于集气瓶口,观察木条是否熄灭进行判断;固体和液体反应不需加热制取气体的装置,还可以用双氧水来制取氧气;
(5)据反应前后原子的种类和数目不变判断物质的化学式;洗气装置中导管要长进导出,澄清石灰水中的溶质氢氧化钙是微溶于水,即便是饱和溶液里面含的氢氧化钙也很少,一般无法除净二氧化碳,而烧碱极易溶于水,水溶液中溶质含量大可应将二氧化碳处理干净;
(6)若进行CO还原CuO的实验,检验气体生成物用澄清的石灰水,处理一氧化碳尾气可用酒精灯点燃,利用其可燃性将其燃烧掉.
点评:本题考查知识综合而全面,同学们要加强基础知识的积累,才能结合具体情景灵活分析解答问题.

练习册系列答案
相关题目
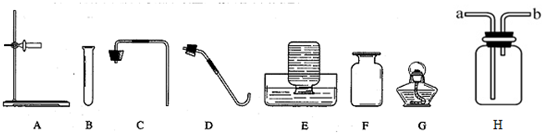
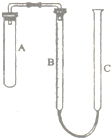 现有实验药品:一定质量的锌(片状或粒状)、浓硫酸(密度1.84g/cm3)、水以及如图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架上,供量气用;C管可上下移动,以调节液面高低.利用此装置可测定锌的相对原子质量.(设锌全部反应,产生的气体不超过50mL).
现有实验药品:一定质量的锌(片状或粒状)、浓硫酸(密度1.84g/cm3)、水以及如图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架上,供量气用;C管可上下移动,以调节液面高低.利用此装置可测定锌的相对原子质量.(设锌全部反应,产生的气体不超过50mL).

