题目内容
科学家预言:“未来最理想的燃料是绿色植物.”即将植物的秸杆[主要成分为纤维素、化学式为(C6H10O5)n],用适当的催化剂与水作用生成葡萄糖(化学式为C6H12O6),再将葡萄糖在一定条件下发酵转化为乙醇(同时有CO2放出),试回答下列问题:
(1)葡萄糖的相对分子质量为______.
(2)纤维素转化为葡萄糖的化学反应方程式为______.
(3)根据你所掌握的乙醇、氢气的化学知识,若让你将这两种物质设计成机动车辆的燃料用料,你认为它们分别有哪些优点和缺点:______.
解:(1)葡萄糖的相对分子质量为:12×6+1×12+16×6=180;
(2)根据纤维素(C6H10O5)n],在适当催化剂催化作用下,与水作用生成葡萄糖(C6H12O6),可知反应物是纤维素和水写在等号的左边,生成物是葡萄糖写在等号的后边,先配平碳和氢,最后配平氧即可,反应条件是催化剂写在等号的上边,所以方程式是:(C6H10O5)n+nH2O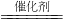 nC6H12O6;
nC6H12O6;
(3)氢气作为能源的优点是:热值高,产物不污染环境,原料丰富;氢气作为能源的缺点是:制取成本高,不容易贮存;乙醇的燃烧产物是二氧化碳和水,所以乙醇作为燃料的一个优点是不污染环境,缺点是燃烧放出的热量少,燃烧生成的二氧化碳会造成温室效应.
故答案为:(1)180;(2)(C6H10O5)n+nH2O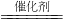 nC6H12O6;(3)氢气作为能源的优点是:热值高,产物不污染环境,原料丰富;氢气作为能源的缺点是:制取成本高,不容易贮存;乙醇的燃烧产物是二氧化碳和水,所以乙醇作为燃料的一个优点是不污染环境,缺点是燃烧放出的热量少,燃烧生成的二氧化碳会造成温室效应.
nC6H12O6;(3)氢气作为能源的优点是:热值高,产物不污染环境,原料丰富;氢气作为能源的缺点是:制取成本高,不容易贮存;乙醇的燃烧产物是二氧化碳和水,所以乙醇作为燃料的一个优点是不污染环境,缺点是燃烧放出的热量少,燃烧生成的二氧化碳会造成温室效应.
分析:(1)根据相对分子质量的计算方法考虑;(2)根据方程式的书写方法考虑;(3)根据乙醇和氢气的元素组成和性质的不同进行分析.
点评:解答本题关键是要知道相对分子质量的计算方法,熟悉化学方程式的书写方法,知道氢气和乙醇的性质差异.
(2)根据纤维素(C6H10O5)n],在适当催化剂催化作用下,与水作用生成葡萄糖(C6H12O6),可知反应物是纤维素和水写在等号的左边,生成物是葡萄糖写在等号的后边,先配平碳和氢,最后配平氧即可,反应条件是催化剂写在等号的上边,所以方程式是:(C6H10O5)n+nH2O
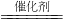 nC6H12O6;
nC6H12O6;(3)氢气作为能源的优点是:热值高,产物不污染环境,原料丰富;氢气作为能源的缺点是:制取成本高,不容易贮存;乙醇的燃烧产物是二氧化碳和水,所以乙醇作为燃料的一个优点是不污染环境,缺点是燃烧放出的热量少,燃烧生成的二氧化碳会造成温室效应.
故答案为:(1)180;(2)(C6H10O5)n+nH2O
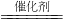 nC6H12O6;(3)氢气作为能源的优点是:热值高,产物不污染环境,原料丰富;氢气作为能源的缺点是:制取成本高,不容易贮存;乙醇的燃烧产物是二氧化碳和水,所以乙醇作为燃料的一个优点是不污染环境,缺点是燃烧放出的热量少,燃烧生成的二氧化碳会造成温室效应.
nC6H12O6;(3)氢气作为能源的优点是:热值高,产物不污染环境,原料丰富;氢气作为能源的缺点是:制取成本高,不容易贮存;乙醇的燃烧产物是二氧化碳和水,所以乙醇作为燃料的一个优点是不污染环境,缺点是燃烧放出的热量少,燃烧生成的二氧化碳会造成温室效应.分析:(1)根据相对分子质量的计算方法考虑;(2)根据方程式的书写方法考虑;(3)根据乙醇和氢气的元素组成和性质的不同进行分析.
点评:解答本题关键是要知道相对分子质量的计算方法,熟悉化学方程式的书写方法,知道氢气和乙醇的性质差异.

练习册系列答案
相关题目