题目内容
【题目】美国普度大学研发出一种制备氢气的新工艺,流程如图所示。铝镓合金是铝和镓熔合在一起的混合物,具有金属特性。铝镓合金与水的反应中生成物是氧化铝、氢气和镓,相当于镓未参加反应,所以实际上发生的反应是:2Al+3H2O═Al2O3+3H2↑
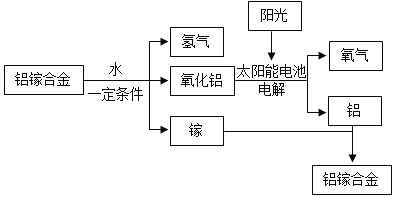
(1)铝镓合金_____导电(填“能”或“不能”)。
(2)铝在常温下能被氧气氧化生成氧化铝,写出该反应的符号表达式_____。
(3)当前工业上常采用电解水制取氢气,反应为2H2O![]() 2H2↑+O2↑,电解水制取氢气需要消耗电能且反应的速度慢,与之相比,由铝镓合金制取氢气的优点是_____。
2H2↑+O2↑,电解水制取氢气需要消耗电能且反应的速度慢,与之相比,由铝镓合金制取氢气的优点是_____。
(4)流程中含有氧元素的物质有_____。
(5)下列说法正确的是_____。
A铝镓合金可以循环利用
B太阳能的利用可以部分解决能源危机问题
C铝镓合金制取氢气的反应属于分解反应
【答案】能 Al+O2![]() Al2O3 不消耗电能,反应速率快 水、氧化铝、氧气 AB
Al2O3 不消耗电能,反应速率快 水、氧化铝、氧气 AB
【解析】
(1)合金具有金属特性,故铝镓合金能导电。
(2)铝在常温下能被氧气氧化生成氧化铝,反应的符号表达式为Al+O2![]() Al2O3。
Al2O3。
(3)当前工业上常采用电解水制取氢气,反应方程式为2H2O![]() 2H2↑+O2↑,电解水制取氢气需要消耗电能且反应的速度慢,与之相比,由铝镓合金制取氢气的优点是不消耗电能,反应速率快。
2H2↑+O2↑,电解水制取氢气需要消耗电能且反应的速度慢,与之相比,由铝镓合金制取氢气的优点是不消耗电能,反应速率快。
(4)流程中含有氧元素的物质有水、氧化铝、氧气。
(5)A、铝镓合金可以循环利用,故A正确;
B、太阳能的利用可以部分解决能源危机问题,故B正确;
C、铝镓合金制取氢气的反应是一种单质和一种化合物生成另一种单质和另一种化合物的反应,属于置换反应,故C不正确。故选AB。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目