题目内容
【题目】氯化钠在自然界中分布很广,海水里含大量氯化钠.某氯化钠粗品中含少量氯化镁和氯化钙,某化学兴趣小组设计提纯方案如下:
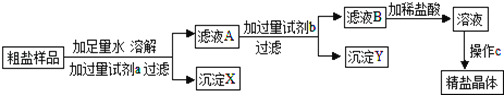
(1)方案中加入过量试剂a若为氢氧化钠溶液,则其目的是为了除去氯化钠粗品中的某种杂质,写出该反应的化学方程式 ;
(2)在过滤操作中,除用到带铁圈的铁架台、烧杯、玻璃棒外,还需要用到玻璃仪器是 ;
(3)方案中加入过量试剂b应为 溶液;
(4)向滤液B滴加稀盐酸的过程中,当观察到溶液的现象为 时,应停止滴加,写出相关的化学方程式 。
(5)操作C的名称为 。
【答案】(1)MgCl2+2NaOH=Mg(OH)2↓+2NaCl (2)漏斗 (3)碳酸钠 (4)不再产生气泡;
NaOH+HCl=NaCl+H2O,Na2CO3+2HCl=2NaCl+H2O+CO2↑ (5)蒸发
【解析】
试题(1)氢氧化钠能和氯化镁反应生成氢氧化镁沉淀和氯化钠,从而把氯化镁除去,反应的化学方程式为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl。
(2)在过滤操作中,除用到带铁圈的铁架台、烧杯、玻璃棒外,还需要用到玻璃仪器是漏斗。
(3)加入碳酸钠溶液时,能够把氯化钙除去,方案中加入过量试剂b应为碳酸钠溶液。
(4)向滤液B滴加稀盐酸的过程中,当观察到溶液中不再产生气泡时,说明已经完全反应;氢氧化钠、碳酸钠和稀盐酸反应的化学方程式分别为:NaOH+HCl=NaCl+H2O,Na2CO3+2HCl=2NaCl+H2O+CO2↑。
(5)蒸发氯化钠溶液时,能够得到氯化钠晶体。

【题目】请从A或B两题中任选一个作答,若两题均作答,按A计分。

A | B |
实验室用高锰酸钾制取氧气的化学方程式是_____。 用装置A、E制取氧气应该等到_______________时再收集。 | (1)实验室制取二氧化碳的化学方程式是_____。 (2)通常用装置C收集二氧化碳的理由是___________________ 。 |
【题目】某化学兴趣小组的同学,通过咨询老师准备用亚硫酸钠溶液与浓硫酸反应来制备一定量的SO2(Na2SO3+H2SO4(浓)==Na2SO4+SO2↑+H2O]。老师给他们提供了一瓶亚硫酸钠溶液并告知该瓶溶液放置时间可能较长,不知是否变质。兴趣小组的同学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
(提出问题)①该瓶溶液中溶质的成分是什么?
②该瓶溶液中亚硫酸钠的质量分数是多少?
(查阅资料)
(1) Na2SO3有较强还原性,在空气中易被氧气氧化:2 Na2SO3+O2==2Na2SO4;
(2) Na2SO3能与酸反应产生SO2气体;
(3)SO32-、SO42-均能与Ba2+反应产生白色沉淀,BaSO3可溶于稀盐酸。
(作出猜想)
猜想1:没有变质,成分是Na2SO3;
猜想2完全变质,成分是Na2SO4;
你认为还可能有的猜想3:_____________________。
(实验探究I)甲、乙两组分别进行实验探究溶液是否变质:
小组 | 实验操作 | 现象 | 结论 |
甲组 | 取少量样品于试管中加入过量稀盐酸; | 产生气泡 | 没有变质,还是Na2SO3 |
乙组 | 取少量样品于试管中加入氯化钡溶液,再加入足量稀盐酸。 | _____ | 已部分变质 |
(评价)有同学质疑甲组方案不合理,理由是___________。
(实验探究II)
甲组设计如下实验测定Na2SO3溶液的溶质质量分数。(注:空气中二氧化碳的影响忽略不计)
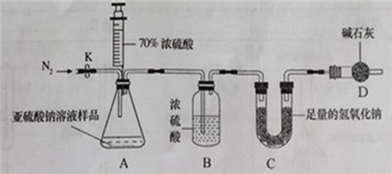
(1)连好装置并检查装置气密性,在锥形瓶中放入126g该样品
(2)实验前称量C装置的质量;
(3)关闭活塞K,用注射器推入浓硫酸至不再产生气泡;
(4)打开活塞K,缓缓鼓入一定量的氮气,关闭活塞K;
(5)再次称量C装置的质量发现比反应前增重6.4g。
由此,计算出该溶液中Na2SO3的质量分数为_____________;
(解释)若没有进行第4步操作,则测得亚硫酸钠溶液的溶质质量分数比实际的____(填”偏小”或”偏大”)。
乙组仍使用第一次实验的原理,进行如下实验测定Na2SO3溶液的溶质质量分数。
第一步:称取试样ag;
第二步:在溶液中加入过量氯化钡溶液和足量稀盐酸;
第三步:过滤、洗涤、烘干沉淀;
第四步:称量沉淀的质量为bg;
第五步:计算溶液中Na2SO3的溶质质量分数=(1-142b/233a)×100%。
试完成下列问题:
(1)加入氯化钡溶液过量的目的是________________;
(2)第三步操作要洗涤沉淀的原因是______________________;
(反思)由此可得出,保存亚硫酸钠时应___________________________。