题目内容
【题目】某实验小组用废黄铜(铜锌合金)为原料制备氯化锌,流程如下:
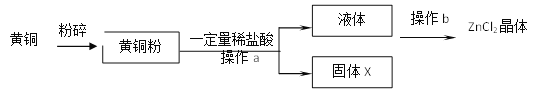
(1)黄铜粉碎的目的是_________________________________。
(2)证明锌已经完全反应的方法和现象是____________,反应的化学方程式____________,属于_______________基本类型的反应。
(3)操作a的名称是___________,实验室中进行此操作时,用到的玻璃仪器除漏斗、烧杯外,还需____________,它的作用 是___________________。
【答案】 增大黄铜与盐酸的接触面积,使其中的锌充分反应完 继续加稀盐酸,若没有气泡产生,证明锌已反应完 Zn+2HCl=ZnCl2+H2↑ 置换反应 过滤 玻璃棒 引流作用
【解析】本题考查了金属的提纯,可根据金属的活动性理解流程图的含义。
根据流程可知:
(1)黄铜粉碎的目的是增加接触面积,使其中的锌充分反应完;
(2)因为锌与稀盐酸反应生成氢气,证明锌已经完全反应的方法和现象是向固体X继续加稀盐酸,若没有气泡产生,证明锌已反应完,反应的化学方程式是Zn+2HCl==ZnCl2+H2↑,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物,属于置换反应;
(3)根据图可知,操作a为分离固体和液体,故其名称是过滤,实验室中进行此操作时,用到的玻璃仪器除漏斗、烧杯外,还需玻璃棒,它的作用是引流。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目