题目内容
【题目】下列化学用语表示正确的是
A. 高锰酸钾的化学式:K2MnO4B. 60个碳原子:C60
C. 2个氯离子:2Cl-D. Mg2+的结构示意图:![]()
【答案】C
【解析】
A、高锰酸钾的化学式为:KMnO4,错误;
B、原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字。故60个碳原子可表示为:60C,错误;
C、离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其符号前加上相应的数字。故2个氯离子可表示为:2Cl-,正确;
D、Mg2+的结构示意图中质子数为12,故Mg2+的结构示意图可表示为:![]() ,错误。
,错误。
故选C。

【题目】学习了MnO2对过氧化氢分解有催化作用的知识后.某同学想:CuO(氧化铜)能否起到类似MnO2的催化剂作用呢?于是进行了以下探究.
(猜想)Ⅰ.CuO不是催化剂,也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后质量和化学性质没有发生改变
(查阅资料)1、很多金属氧化物能做过氧化氢的催化剂,例如:MnO2、CuO、氧化铁(Fe2O3)等。
2、过氧化氢有很强的氧化性,能使有色布条褪色,能使铁等金属生锈(铁锈的主要成分是氧化铁),能用于伤口杀菌消毒等。
(实验)用天平称量0.2g CuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
实验步骤3现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
_____,带火星的木条复燃. | _____ | 溶液中有气泡放出, __________ | 猜想Ⅰ、Ⅱ不成立;猜想Ⅲ成立 |
(2)步骤1的目的是_____;
(3)步骤④需用到的玻璃仪器有:_____;
(4)过氧化氢能被CuO催化分解放出O2的文字表达式为_____。
(反思)
(5)同学通过实验验证了CuO能做过氧化氢分解的催化剂,另一同学将一根洁净的铁丝放入过氧化氢溶液中开始没有明显现象,过一会发现有大量气泡产生。产生这一现象的原因可能是_____,
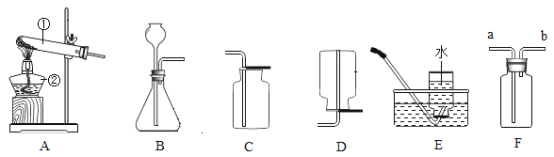
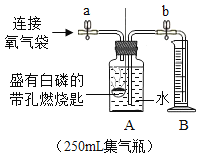
(6)某同学利用下图装置验证空气中氧气的体积分数,将装有足量红磷的燃烧匙置于瓶内中间,并把装有足量白磷的燃烧匙浸没在蒸馏水下。图乙表示用氧气传感器测量的容器内氧气浓度变化曲线图。

(提出问题)红磷在烧瓶内熄灭后,瓶中是否有氧气剩余?
(猜想假设)猜想:①有氧气剩余;②无氧气剩余。
(实验验证)待装置完全冷却后,将装有白磷的燃烧匙提出水面,用激光笔点燃白磷。
(得出结论)分析图乙得出,猜想②正确
(反思交流)①根据本实验的结论,教材中用“燃烧红磷测定空气中氧气含量”的方法是否可行并说明理由_____。
②曲线DE段氧气浓度变化的主要原因是_____。
③丙图利用铁粉除去氧气较彻底最后生成了氢氧化亚铁。请写出文字表达式_____。
【题目】碳酸氢钠(NaHCO3)是焙制糕点所用的发酵粉的主要成分之一。青竹湖化学兴趣小组的同学们,对 NaHCO3固体的加热分解展开探究。
(提出问题)碳酸氢钠固体加热分解的产物是什么?
(查阅资料)①碳酸氢钠固体受热不稳定,易分解生成碳酸钠(Na2CO3)等
②Na2CO3固体受热不易分解
③CO2能使澄清石灰水变浑浊,而CO不能
(做出猜想)猜想一:产物是Na2CO3、H2O、CO2
猜想二:产物是Na2CO3、H2O、CO
(实验探究)实验操作
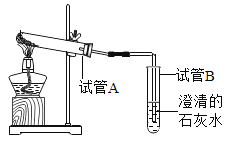
实验操作 | 现象 | 结论 |
如上图,取8.4g干燥的碳酸氢钠粉末于试管A中,用酒精灯加热至固体质量不再变化。 | A试管口出现大量水珠 | 产物中有_____ |
B试管中_____ | 产物中有CO2 |
(实验结论)猜想一成立。
(交流与讨论)
(1)小氧同学在实验结束后,先熄灭酒精灯,后将导管移出试管B他这样操作可能导致的后果是_____。
(2)小硅同学在实验结束后,通过计算得出试管A中剩余固体(不含水分)的质量为_____g。
(3)小铝同学提出不需要进行实验探究,从理论上分析就能知道猜想二不成立,他的理由是_____。
(4)小铁同学想除去混在Na2CO3固体中的少量 NaHCO3杂质,从而得到纯净的Na2CO3固体。请你结合以上实验探究的结论,帮助小铁同学设计一个简单且合理的实验方案:_____(简单描述实验操作即可)。
【题目】学习化学离不开实验探究。请利用学过的化学知识完成下列实验探究。
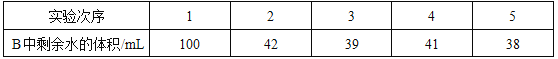
(一)某同学根据铁生锈的原理,用铁粉测定空气中氧气的含量,设计了如图实验,充分反应后测得数据如表:
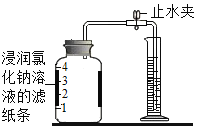
实验前的体积 | 实验后的体积 | |
集气瓶内空气 | 量筒内水 | 量筒内剩余水 |
250mL | 180.0mL | 129.5mL |
实验时该同学不是将铁粉堆在瓶底,而是将铁粉撒在浸润了氯化钠溶液的滤纸条上,再把该滤纸条贴在广口瓶内侧,其目的是________________,氯化钠溶液的作用是_________________。根据表中数据计算得出空气中氧气的体积分数为_____________(结果保留到0.1%)。与用红磷燃烧的方法相比,用该方法测定空气中氧气含量的主要优点:一是没有污染,二是_________________。
(二)为了探究二氧化碳的性质,某同学设计了如下图所示的实验:
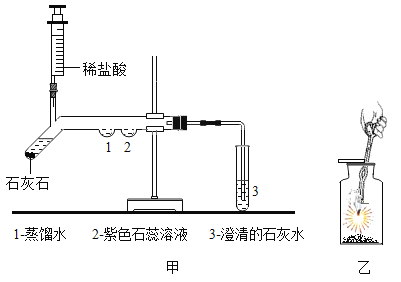
(1)用注射器注入稀盐酸,一段时间后,可观察到在1、2两处中有一处有明显的现象发生,发生该实验现象的符号表达式为__________________;该反应属于__________反应(填化合或分解)
(2)3处的澄清石灰水变浑浊,该反应的符号表达式为_________________;
(3)如图乙,将点燃的镁条伸入二氧化碳中,观察到镁条继续燃烧,请你写出一个对燃烧的新认识___________________.
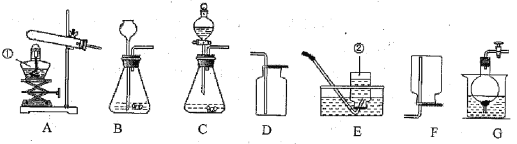
(三)为了测定蜡烛中碳、氢两种元素的质量比,某化学兴趣小组设计了如图所示的实验,实验步骤如下:先分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量.(注:浓硫酸只吸收水分,氢氧化钠和氧化钙可吸收水也可吸收二氧化碳)按图示连接好仪器.点燃蜡烛,同时从a导管口抽气,一段时间后熄灭蜡烛,再分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量,实验数据如表.
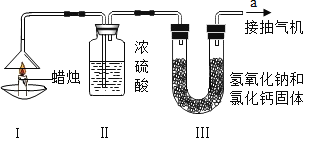
蜡烛 | 装置Ⅱ | 装置Ⅲ | |
反应前的质量/g | 15.8 | 182.3 | 212.2 |
反应后的质量/g | 14.4 | 184.1 | 216.6 |
(1)该实验中测得水的质量为___________g,二氧化碳的质量为___________g.
(2)由该实验数据计算,蜡烛中碳、氢元素的质量之比为___________.
(3)装置Ⅱ和装置Ⅱ的顺序能否颠倒:___________(填“能”或“不能”)
(4)理论上,装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛失去的质量,其原因是___________.