题目内容
用化学符号表示:
①5个磷原子
②氯气
③氢氧根离子
④3个亚铁离子
⑤氯化钠
⑥氢氧化铜中铜元素的化合价
(OH)2
(OH)2
⑦大理的主要成分
⑧氢氧化铁
①5个磷原子
5P
5P
②氯气
Cl2
Cl2
③氢氧根离子
OH-
OH-
④3个亚铁离子
3Fe2+
3Fe2+
⑤氯化钠
NaCl
NaCl
⑥氢氧化铜中铜元素的化合价
| +2 |
| Cu |
| +2 |
| Cu |
⑦大理的主要成分
CaCO3
CaCO3
⑧氢氧化铁
Fe(OH)3
Fe(OH)3
.分析:本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答:解:①原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.所以5个磷原子,就可表示为5P;
②氯气是由氯气分子构成的,其化学式为:Cl2;
③由离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.氢氧根离子可表示
为:OH-;
④离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,故3个亚铁离子3Fe2+;
⑤氯化钠是由显+1价的钠元素和显-1价的氯元素组成的,根据化合价原则,其化学式可表示为:NaCl;
⑥根据元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,因此氢氧化铜中铜元素的化合价为+2价表示为:
(OH)2;
⑦大理石的主要成分为碳酸钙,是由显+2价的钙元素和显-2价的碳酸根组成的,根据化合价原则,其化学式可表示为:CaCO3;
⑧氢氧化铁是由显+3价的铁元素和显-1价的氢氧根组成,根据化合价原则,其化学式可表示为:Fe(OH)3;
故答案为:①5P;②Cl2;③OH-;④3Fe2+;⑤NaCl;⑥
(OH)2;⑦CaCO3;⑧Fe(OH)3;
②氯气是由氯气分子构成的,其化学式为:Cl2;
③由离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.氢氧根离子可表示
为:OH-;
④离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,故3个亚铁离子3Fe2+;
⑤氯化钠是由显+1价的钠元素和显-1价的氯元素组成的,根据化合价原则,其化学式可表示为:NaCl;
⑥根据元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,因此氢氧化铜中铜元素的化合价为+2价表示为:
| +2 |
| Cu |
⑦大理石的主要成分为碳酸钙,是由显+2价的钙元素和显-2价的碳酸根组成的,根据化合价原则,其化学式可表示为:CaCO3;
⑧氢氧化铁是由显+3价的铁元素和显-1价的氢氧根组成,根据化合价原则,其化学式可表示为:Fe(OH)3;
故答案为:①5P;②Cl2;③OH-;④3Fe2+;⑤NaCl;⑥
| +2 |
| Cu |
点评:本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础.

练习册系列答案
相关题目
根据如图填空:
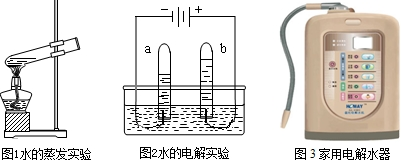
(1)图2实验的化学方程式为 ;
(2)比较图1和图2两个实验中水的变化,用分子原子的观点分析其不同点:
;
(3)在图2实验通电时,a试管中液体呈碱性、b试管中液体呈酸性,利用此原理设计的家用电解水器(图3),可得酸碱性不同的水,且各有其用途(见图表).①右表中用于“日常饮用”的水遇紫色石蕊试液显 色;
②家用电解水器生成的碱性水可除去水中有害的重金属离子,生成小分子团水,因而对健康有益.请用化学符号表示含5个水分子的水分子团: ;
③图2装置电解实验完毕,测定剩余水的pH,结果与实验前相同.请对此现象可能的原因提出一个合理的猜想: .

(1)图2实验的化学方程式为
(2)比较图1和图2两个实验中水的变化,用分子原子的观点分析其不同点:
(3)在图2实验通电时,a试管中液体呈碱性、b试管中液体呈酸性,利用此原理设计的家用电解水器(图3),可得酸碱性不同的水,且各有其用途(见图表).①右表中用于“日常饮用”的水遇紫色石蕊试液显
| pH | 水的应用 |
| 10.0 | 浸泡蔬菜 |
| 9.5 | 日常饮用 |
| 9.0 | 烹饪 |
| 6.0 | 洗头发 |
| 5.5 | 洗涤器皿 |
③图2装置电解实验完毕,测定剩余水的pH,结果与实验前相同.请对此现象可能的原因提出一个合理的猜想:

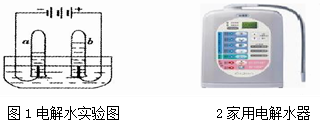 (2010?密云县一模)水是生命之源,2010 年世界水日的主题是“关注水质、抓住机遇、应对挑战”.
(2010?密云县一模)水是生命之源,2010 年世界水日的主题是“关注水质、抓住机遇、应对挑战”.