题目内容
(2012?长春)同学们通过以下在溶液中进行的实验,探究复分解反应发生的条件:
①H2SO4+Ba(NO3)2
②H2SO4+NaOH
③H2SO4+Na2CO3
④Ba(NO3)2+NaOH
⑤Ba(NO3)2+Na2CO3
⑥NaOH+Na2CO3
(1)同学们总结归纳出复分解反应发生的条件是生成物中有
(2)同学们将实验后的所有物质倒入同一烧杯中,后续实验及现象如下:
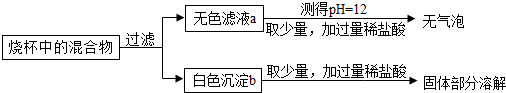
综合分析可知,无色滤液a中一定含有的溶质包括
(3)下列有关利用无色滤液a和白色沉淀b的设想中,合理的是
A.鉴别MgCl2溶液和BaCl2溶液:取样,滴加无色滤液a
B.制NaNO3溶液:向无色滤液a中加入适量的稀HNO3
C.除去Ba(NO3)2溶液中的HNO3:向其中加入过量的白色沉淀b.
①H2SO4+Ba(NO3)2
②H2SO4+NaOH
③H2SO4+Na2CO3
④Ba(NO3)2+NaOH
⑤Ba(NO3)2+Na2CO3
⑥NaOH+Na2CO3
(1)同学们总结归纳出复分解反应发生的条件是生成物中有
沉淀、气体、水
沉淀、气体、水
;(2)同学们将实验后的所有物质倒入同一烧杯中,后续实验及现象如下:

综合分析可知,无色滤液a中一定含有的溶质包括
NaOH
NaOH
和NaNO3
NaNO3
;(3)下列有关利用无色滤液a和白色沉淀b的设想中,合理的是
C
C
.A.鉴别MgCl2溶液和BaCl2溶液:取样,滴加无色滤液a
B.制NaNO3溶液:向无色滤液a中加入适量的稀HNO3
C.除去Ba(NO3)2溶液中的HNO3:向其中加入过量的白色沉淀b.
分析:(1)根据沉淀、气体、水是复分解反应发生的条件进行解答;
(2)根据反应后生成的物质以及实验现象进行解答;
(3)根据无色滤液a和白色沉淀b的成分进行解答.
(2)根据反应后生成的物质以及实验现象进行解答;
(3)根据无色滤液a和白色沉淀b的成分进行解答.
解答:解:(1)复分解反应发生的条件是生成物中有沉淀、气体、水生成;
(2)根据滤液中pH值为12,显碱性,加入盐酸没有气体说明无色滤液a中一定含有的溶质NaOH、NaNO3;
(3)白色沉淀b加入过量稀盐酸,部分溶解,说明沉淀中含有硫酸钡和碳酸钡,所以无色滤液a和白色沉淀b的设想中,合理的是除去Ba(NO3)2溶液中的HNO3:向其中加入过量的白色沉淀b.
故答案为:(1)沉淀、气体、水; (2)NaOH、NaNO3;(3)C.
(2)根据滤液中pH值为12,显碱性,加入盐酸没有气体说明无色滤液a中一定含有的溶质NaOH、NaNO3;
(3)白色沉淀b加入过量稀盐酸,部分溶解,说明沉淀中含有硫酸钡和碳酸钡,所以无色滤液a和白色沉淀b的设想中,合理的是除去Ba(NO3)2溶液中的HNO3:向其中加入过量的白色沉淀b.
故答案为:(1)沉淀、气体、水; (2)NaOH、NaNO3;(3)C.
点评:本题考查复分解反应及其反应条件.是化学中四大基本反应类型之一.它的概念是两种化合物互相交换成分,生成两种新的化合物的反应.沉淀、气体、水是复分解反应发生的条件.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案
相关题目

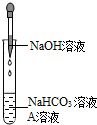 (2012?北京)同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
(2012?北京)同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应. (2012?巴中)同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行了探究.
(2012?巴中)同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行了探究.