题目内容
 2013年我国纪念“世界水日”和“中国水周”活动的主题是“节约保护水资源,大力建设生态文明”.某化学兴趣小组进行了一系列兴趣小实验.
2013年我国纪念“世界水日”和“中国水周”活动的主题是“节约保护水资源,大力建设生态文明”.某化学兴趣小组进行了一系列兴趣小实验.(1)取回大明湖水样,静置后过滤.在实验室里,过滤需要用到的玻璃仪器有
(2)食盐是生活必需品,兴趣小组同学进行粗盐提纯实验,主要经过以下操作步骤:称量→溶解→
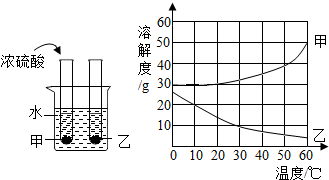
(3)甲、乙两种固体的溶解度曲线如图所示.现将两支分别装有甲、乙两物质饱和溶液的试管(底部均有少量未溶解的固体)浸入盛有水的烧杯中,再向烧杯中加入一定量的浓硫酸.
①30℃时,甲、乙两种饱和溶液的溶质质量分数为:甲
②烧杯中加入浓硫酸后,试管中固体质量增加的是
分析:(1)依据过滤所用玻璃仪器回答;
(2)据粗盐提纯的一般步骤回答;
(3)①据饱和溶液中溶质的质量分数=
×100%可知:溶解度越大,饱和溶液中溶质的质量分数越大;
②浓硫酸溶于水放热,试管中固体质量增加,说明该物质的溶解度随温度的升高而减小,据此结合溶解度曲线分析解答.
(2)据粗盐提纯的一般步骤回答;
(3)①据饱和溶液中溶质的质量分数=
| 溶解度 |
| 100g+溶解度 |
②浓硫酸溶于水放热,试管中固体质量增加,说明该物质的溶解度随温度的升高而减小,据此结合溶解度曲线分析解答.
解答:解:(1)在实验室里,过滤需要用到的玻璃仪器有玻璃棒、烧杯、漏斗,故取回大明湖水样,静置后过滤,还需要的玻璃仪器是烧杯;
(2)粗盐提纯实验的主要操作步骤是:称量、溶解、过滤、蒸发、再次称量、计算产率;
(3)①30℃时,甲的溶解度大于乙的溶解度,所以甲、乙两种饱和溶液的溶质质量分数为:甲大于乙;
②浓硫酸溶于水放热,试管中固体质量增加,说明该物质的溶解度随温度的升高而减小,乙的溶解度随温度的升高而减小,故烧杯中加入浓硫酸后,试管中固体质量增加的是乙;原因是:浓硫酸溶于水放出热量,温度升高,乙的溶解度降低,所以固体质量增加;
故答案为:(1)烧杯;(2)过滤;(3)①大于; ②乙;浓硫酸溶于水放出热量,温度升高,乙的溶解度降低,所以固体质量增加(合理答案均可).
(2)粗盐提纯实验的主要操作步骤是:称量、溶解、过滤、蒸发、再次称量、计算产率;
(3)①30℃时,甲的溶解度大于乙的溶解度,所以甲、乙两种饱和溶液的溶质质量分数为:甲大于乙;
②浓硫酸溶于水放热,试管中固体质量增加,说明该物质的溶解度随温度的升高而减小,乙的溶解度随温度的升高而减小,故烧杯中加入浓硫酸后,试管中固体质量增加的是乙;原因是:浓硫酸溶于水放出热量,温度升高,乙的溶解度降低,所以固体质量增加;
故答案为:(1)烧杯;(2)过滤;(3)①大于; ②乙;浓硫酸溶于水放出热量,温度升高,乙的溶解度降低,所以固体质量增加(合理答案均可).
点评:了解过滤、粗盐提纯的一般步骤、所用仪器,明确浓硫酸溶于水放热,并能结合物质的溶解度曲线分析解答相关问题,较好考查学生对知识的掌握和应用,难度不大.

练习册系列答案
相关题目
 联合国确定2013年“世界水日”的宣传主题是“水合作”.我国纪念2013年“世界水日”和“中国水周”活动的宣传主题为“节约保护水资源,大力建设生态文明”.请根据下列提示回答问题:
联合国确定2013年“世界水日”的宣传主题是“水合作”.我国纪念2013年“世界水日”和“中国水周”活动的宣传主题为“节约保护水资源,大力建设生态文明”.请根据下列提示回答问题: 2013年我国纪念“世界水日”和“中国水周”活动的主题是“节约保护水资源,大力建设生态文明”.某化学兴趣小组进行了一系列兴趣小实验.
2013年我国纪念“世界水日”和“中国水周”活动的主题是“节约保护水资源,大力建设生态文明”.某化学兴趣小组进行了一系列兴趣小实验. 和“中国水周”活动的主题是“节约保护水资源,大力建设生态文明”。某化学兴趣小组进行了一系列兴趣小实验。源:Z。xx。k.Co
和“中国水周”活动的主题是“节约保护水资源,大力建设生态文明”。某化学兴趣小组进行了一系列兴趣小实验。源:Z。xx。k.Co 滤需要用到的玻璃仪器有
滤需要用到的玻璃仪器有 
 ②烧杯中加入浓硫酸后,试管中固体质量增加的是
②烧杯中加入浓硫酸后,试管中固体质量增加的是  。
。