题目内容
【题目】如图所示为实验室中常见的气体制备、净化、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器).试根据题目要求,回答下列问题: 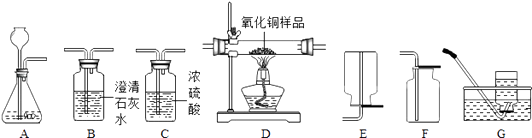
(1)若用锌粒和稀盐酸(盐酸具有挥发性)反应制取并收集干燥的氢气. ①制取并收集干燥的氢气所选仪器的连接顺序为(填写仪器序号字母).
②制取氢气的反应方程式为
(2)小明同学欲测定水煤气中一氧化碳和氢气含量(含少量二氧化碳和水蒸气),所选仪器的连接顺序为:B→C→D→C→B. ①写出装置B中发生反应的化学方程式 .
②装置D中观察到的实验现象是 .
③小明同学的设计方案有一明显的不足,这样操作可能造成的后果是 .
【答案】
(1)ABCE;Zn+2HCl═ZnCl2+H2↑
(2)Ca(OH)2+CO2═CaCO3↓+H2O;黑色固体变为红色固体;没有尾气处理装置,会污染空气
【解析】解:(1)①用锌粒和稀盐酸(盐酸具有挥发性)反应制取氢气用A装置,盐酸挥发氯化氢气体,混有的氯化氢气体用澄清的石灰水除去,干燥用浓硫酸,氢气密度比空气小,用向下排空气法收集,而气体从溶液中出来会带来水蒸气,所以要先除杂再干燥,然后收集,故制取并收集干燥的氢气所选仪器的连接顺序为ABCE;②铁和稀盐酸反应生成氯化亚铁和氢气,方程式是Fe+2HCl═FeCl2+H2↑;(2)①装置B中发生反应是二氧化碳与澄清石灰水的反应,二者反应生成碳酸钙沉淀和水,方程式是:Ca(OH)2+CO2═CaCO3↓+H2O;②一氧化碳具有还原性,可将黑色的氧化铜还原为红色的铜;③小明未设计尾气处理装置,会使未参加反应的一氧化碳排放到空气中污染空气; 所以答案是:(1)①ABCE; ②Fe+2HCl═FeCl2+H2↑;(2)①Ca(OH)2+CO2═CaCO3↓+H2O;②黑色固体变为红色固体; ③没有尾气处理装置,会污染空气.
【考点精析】解答此题的关键在于理解一氧化碳的性质的相关知识,掌握一氧化碳的物理性质:无色,无味的气体,密度比空气略小,难溶于水;一氧化碳的化学性质:可燃性和还原性,以及对氢气的制取和检验的理解,了解氢气的实验室制法原理:Zn + H2SO4 = ZnSO4 +H2↑;Zn + 2HCl = ZnCl2 +H2↑不可用浓盐酸的原因 浓盐酸有强挥发性 ;不可用浓硫酸或硝酸的原因 浓硫酸和硝酸有强氧化性.

 阅读快车系列答案
阅读快车系列答案