题目内容
【题目】清回答下列有关金属材料的问题.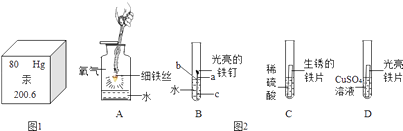
(1)在元素周期表中,汞元素的信息如图1所示,下列对图中信息解释正确的是 .
A.汞属于金属元素
B.汞原子核外电子数是200.6
C.汞原子核内中子数是80
D.汞原子的相对原子质量是80
(2)下列是与铁的性质有关的部分实验图图2:
①A中细铁丝燃烧生成的黑色固体物质的化学式是 .
②B中铁钉最易生锈的部位是(填“a”、“b”或“c”).
③C中刚开始无气泡产生,溶液颜色逐渐由无色变为黄色,此时试管内发生反应的化学方程式是 .
④D中反应一段时间后,试管内溶液质量与反应前相比(填“增大”、“不变”或“减小”).
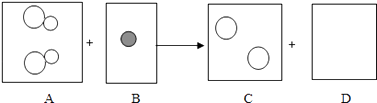
(3)在AgNO3、Al(NO3)3、Cu(NO3)2的混合溶液中加入一定量的锌粉,充分反应后过滤,得到溶液甲和固体乙,溶液甲成蓝色.
①固体乙中一定含有 , ②溶液甲中含有的阳离子为 .
(4)为测定某Cu﹣Zn合金中铜的质量分数,某同学将10g该合金放入到盛有40g足量稀硫酸的烧杯中,充分反应后,测得烧杯中剩余物质的质量为49.9g,请计算原合金中铜的质量分数.
【答案】
(1)A,B
(2)Fe3O4;b;Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;减小
(3)银;Cu2+、Al3+、Zn2+
(4)
解:根据质量守恒定律,产生氢气的质量为:10g+40g﹣49.9g=0.1g;
设黄铜样品中锌的质量为x,
Zn+ | H2SO4 | ═ | ZnSO4+ | H2↑ |
65 | 2 | |||
x | 0.1g |
![]() =
=![]()
解得:x=3.25g黄铜样品中铜的质量分数为: ![]() =67.5%
=67.5%
【解析】解:(1)A、汞属于金属元素,说法正确;
B、汞原子核外电子数是200.6,说法正确;
C、汞原子核内中子数不能确定,说法不正确;
D、汞原子的原子序数是80.说法不正确;(2)①铁丝的燃烧产物是四氧化三铁,四氧化三铁是黑色的固体,化学式是:Fe3O4;
②铁生锈的条件:铁与水和氧气同时接触,所以因b处与水和氧气同时充分接触,所以最易生锈.
③未打磨的铁片表面含有锈,锈与硫酸反应产生硫酸铁是黄色的溶液,故反应的方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
④铁和硫酸铜反应产生硫酸亚铁和铜,试管内固体质量比反应前增大,根据质量守恒定律,试管内溶液质量与反应前相比减小.(3)根据金属活动性由强到弱的顺序为铝>锌>铜>银,向溶液中加入一定量的锌粉,锌先与硝酸银反应,当硝酸银完全反应后,再与硝酸铜反应,锌不能与硝酸铝反应.根据溶液甲成蓝色,则滤溶液中仍含有硝酸铜,说明了锌完全参加反应没有剩余,滤渣中一定有银可能含有铜,滤液中一定含有硝酸铝、硝酸锌和硝酸铜,可能含有硝酸银,所以含有的阳离子为Cu2+、Al3+、Zn2+ .
故答为:(1)AB;(2)①Fe3O4;②b;③Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;④减小;(3)银,Cu2+、Al3+、Zn2+;(4)黄铜样品中铜的质量分数为67.5%.
【考点精析】关于本题考查的金属材料的选择依据和书写化学方程式、文字表达式、电离方程式,需要了解黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属;注意:a、配平 b、条件 c、箭号才能得出正确答案.