��Ŀ����
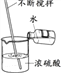
����Ŀ��ʵ������һ����ɫ��ĩ�����ʵ�����֤���˰�ɫ��ĩ A �ijɷֶ��Ǽ���(�� ������Ԫ��)���й���������ͼ��ʾ��
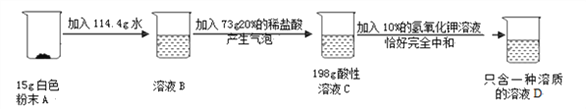
(1)д�����в������ݵķ�Ӧ��ѧ����ʽ ___________��
(2)������֪�����г�A�вμӷ�Ӧ�Ĺ�������(x)�ı���ʽ ___________ ��
(3)A�м��γɷֵĻ�ѧʽΪ ________________________��
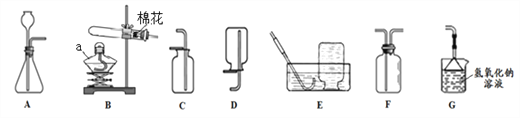
( 4 ) �� �� �� �� �� �� �� �� �� �� �� �� �� Һ �� ǡ �� �� �� �� C �� �� �� �� �� �� �� �� �� �� �� _________________________ ��
(5)�������� D ��Һ�����ʵ���������Ϊ _______________ ��
���𰸡� K2CO3+2HCl=2KCl+H2O+CO2�� 138/44=x/4.4g K2CO3��KCl �Ȼ����� 7.3g ������ 0g���Ȼ����� 16.1g ������ 31g 10%
��������(1)̼�����ܺ����ᷴӦ���ɶ�����̼�����Ұ�ɫ��ĩ A �ijɷֶ��Ǽ��Σ��ʲ������ݵķ�Ӧ��ѧ����ʽΪ��K2CO3+2HCl=2KCl+H2O+CO2����(2)���������غ㶨�ɣ���Ӧ�����ɶ�����̼���������Ϊ��15g+114.4g+73g-198g=4.4g����μӷ�Ӧ��̼��ص�����Ϊ![]() ��
��
K2CO3+2HCl=2KCl+H2O+CO2��
138 44
![]() 4.4g
4.4g
![]() ��
��![]() =13.8g
=13.8g
(3)�ɰ�ɫ��ĩ������Ϊ15 g�Լ�̼���ƺ����ᷴӦ��ֻ��һ�����ʿ�֪��A�м��λ������Ȼ�����������Ϊ15g-13.8g=1.2g����A�ɷֵĻ�ѧʽΪ��K2CO3��KCl��( 4 )�������Ȼ��ص�����Ϊy���μӷ�Ӧ���Ȼ�������Ϊz��
K2CO3+2HCl=2KCl+H2O+CO2��
73 149 44
z y 4.4g
![]() ��y=14.9g��z=7.3g
��y=14.9g��z=7.3g
��C���Ȼ��ص�����Ϊ1.2g+14.9g=16.1g���������֪���μӷ�Ӧ���Ȼ��������Ϊ��![]() ��
��
��������������ط�Ӧ�����Ȼ��ص�����Ϊm���μӷ�Ӧ��������������n��
HCl+KOH=KCl+H2O
36.5 56 74.5
7.3g n m
![]() ��m=14.9g ��n=11.2g
��m=14.9g ��n=11.2g
�ʷ�Ӧ���Ȼ��ص�������Ϊ16.1g+14.9g=31g������ �� �� �� �� �� �� �� Һ �� ǡ �� �� �� �� C �� �� �� �� �� �� �� �� �� �� ���Ȼ����� 7.3g ������ 0g���Ȼ����� 16.1g ������ 31g��(5)���� D ��Һ�����ʵ���������Ϊ��![]() ��
��