题目内容
【题目】银铜合金广泛用于航空工业,切割废料中回收银并制备铜化工产品的工艺流程如图所示:【已知Al(OH)3和Cu(OH)2开始分解的温度分别为450℃ 和80℃ ,Al(OH)3和NaOH能发生反应NaAlO2和水。】
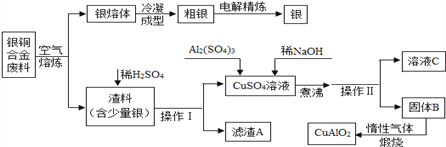
(1)写出铜银合金废料在空气中熔炼时的化学反应方程式___________________。
(2)操作Ⅰ的名称为____________。
(3)写出向CuSO4溶液中加入Al2(SO4)3和稀NaOH其中的一个化学反应方程式____________,其基本反应类型为__________________。
(4)固体混合物B的组成为______;在生成固体B的过程中,必须控制NaOH的加入量,原因是_________。
(5)煅烧固体B获得CuAlO2时通入惰性气体的作用______________,CuAlO2中铜元素的化合价为________价。
【答案】 2Cu +O2![]() 2CuO 过滤 Al2(SO4)3+6NaOH= 3Na2SO4+2 Al(OH)3↓或 CuSO4+2NaOH= Na2SO4+Cu(OH)2↓ 复分解反应 Al(OH)3和CuO 防止Al(OH)3和NaOH发生反应 作保护气 +1
2CuO 过滤 Al2(SO4)3+6NaOH= 3Na2SO4+2 Al(OH)3↓或 CuSO4+2NaOH= Na2SO4+Cu(OH)2↓ 复分解反应 Al(OH)3和CuO 防止Al(OH)3和NaOH发生反应 作保护气 +1
【解析】本题是以从废料中回收银,并制备铜化工产品为背景,考查了混合物的分离、碱和盐的性质等知识。
(1) 在空气中进行熔炼时,铜能和空气中的氧气反应生成氧化铜,化学反应方程式2Cu +O2![]() 2CuO;
2CuO;
(2)操作Ⅰ的结果是把固体和液体分离。操作Ⅰ的名称为过滤;
(3) Al2(SO4)3与NaOH发生复分解反应生成Na2SO4和 Al(OH)3;CuSO4与 NaOH发生复分解反应生成Na2SO4和Cu(OH)2; CuSO4溶液中加入Al2(SO4)3和稀NaOH其中的一个化学反应方程式是 Al2(SO4)3+6NaOH= 3Na2SO4+2 Al(OH)3↓或 CuSO4+2 NaOH= Na2SO4+Cu(OH)2↓;
(4) CuSO4溶液中加入Al2(SO4)3和稀NaOH生成了Al(OH)3 和Cu(OH)2,经煮沸Cu(OH)2分解为氧化铜和水,固体混合物B的组成为Al(OH)3和CuO;Al(OH)3和NaOH能发生反应NaAlO2和水。在生成固体B的过程中,必须控制NaOH的加入量,原因是防止Al(OH)3和NaOH发生反应;
(5) 惰性气体化学性质稳定可用作反应的保护气。煅烧固体B获得CuAlO2时通入惰性气体的作用作保护气;设:铜元素的化合价为x,则有x+(+3)×1+(-2)×2=0,x=+1,CuAlO2中铜元素的化合价为+1价。

 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案