题目内容
【题目】图是某化肥的标签,试根据相关信息计算:

(1)(NH4)2SO4的相对分子质量为_____________
(2)(NH4)2SO4中氮、氢、硫、氧四种元素的原子个数比为 _____________
(3)硫酸铵中氮元素的质量分数_________;并判断该化肥是纯净物还是混合物,是_____。
(4)13.2kg硫酸铵与 _______kg硝酸铵(NH4NO3)中所含氮元素质量相等。
【答案】132 2:8:1:4 21.2% 混合物 8
【解析】
(1)(NH4)2SO4的相对分子质量为(14+1×4)×2+32+16×4=132,故填132;
(2)(NH4)2SO4中氮、氢、硫、氧四种元素的原子个数比为2:8:1:4,故填2:8:1:4;
(3)硫酸铵中氮元素的质量分数为![]() ×100%≈21.2%,故填21.2%;
×100%≈21.2%,故填21.2%;
该化肥中的含氮量为20%<21.2%,所以该化肥为混合物,故填混合物。
(4)解:设硝酸铵的质量为x
13.2kg×![]() ×100%=x×
×100%=x×![]() ×100%
×100%
x=8kg
答:13.2kg硫酸铵与 8kg硝酸铵中所含氮元素质量相等。

 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案【题目】溶液在日常生活和生产中应用广泛,请回答下列问题;
(1)糖水、生理盐水、白酒都是溶液。它们的共同点是:_________、_________、混合物。
(2)写出下列溶液中溶质的化学式:盐酸________、澄清石灰水________、碘酒________、
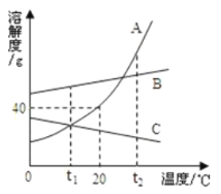
(3)K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下:
温度/℃ | 20 | 30 | 50 | 60 | 80 | |
溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |
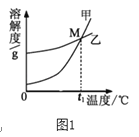
① 图1中能表示KNO3溶解度曲线的是_______(填“甲”或“乙”)。
② 若甲中混有少量的乙,最好采用__________方法提纯甲
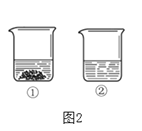
(4)60℃时,向两个分别盛有相同质量的K2CO3和KNO3的烧杯中,各加入100g水,充分溶解后,恢复至60℃,其结果如图2所示。则烧杯①中的溶质是______,此时烧杯①溶液的溶质质量分数为_______。