题目内容
(2013?宿迁)某同学对生铁的组成进行研究.称取生铁样品40g,把500g稀硫酸分5次加入样品中,测得实验数据见下表:(生铁中的杂质不溶于水,也不和稀硫酸反应)
(1)第4次剩余固体的质量m=
(2)该生铁样品中铁的质量分数为
(3)计算所用稀硫酸的溶质质量分数.
| 实验序号 | 加入稀硫酸的质量/g | 剩余固体的质量/g |
| 第1次 | 100 | 28.8 |
| 第2次 | 100 | 17.6 |
| 第3次 | 100 | 6.4 |
| 第4次 | 100 | m |
| 第5次 | 100 | 1.2 |
1.2
1.2
g.(2)该生铁样品中铁的质量分数为
97%
97%
.(3)计算所用稀硫酸的溶质质量分数.
分析:根据表中的数据对比分析可知,每100g的硫酸完全反应,反应掉的铁的质量是11.2g,由于在第四次时剩余混合物的质量总共有6.4g,硫酸有剩余,由第五次剩余的杂质是1.2g,则在四次时,m的质量为1.2g;由此可以求出铁的质量,继而求出铁的质量分数;根据每100g的硫酸完全反应,反应掉的铁的质量是11.2g,可求出每100g的硫酸中溶质的质量,再求出所用稀硫酸的溶质质量分数.
解答:解:(1)由表中的数据对比分析可知,第4次剩余固体的质量m=1.2g;
(2)该生铁样品中铁的质量分数为:
×100%=97%;
(3)设每100g硫酸溶液中溶质质量为x,反应掉的铁的质量为:40g-28.8g=11.2g.
Fe+H2SO4=FeSO4+H2↑
56 98
11.2g x
=
解得:x=19.6g
所用稀硫酸的溶质质量分数是:
×100%=19.6%
故答为:(1)1.2;(2)97%;(3)所用稀硫酸的溶质质量分数是19.6%.
(2)该生铁样品中铁的质量分数为:
| 40g-1.2g |
| 40g |
(3)设每100g硫酸溶液中溶质质量为x,反应掉的铁的质量为:40g-28.8g=11.2g.
Fe+H2SO4=FeSO4+H2↑
56 98
11.2g x
| 56 |
| 98 |
| 11.2g |
| x |
所用稀硫酸的溶质质量分数是:
| 19.6g |
| 100g |
故答为:(1)1.2;(2)97%;(3)所用稀硫酸的溶质质量分数是19.6%.
点评:本道题主要考查的是根据化学方程式的计算,解答本题的关键是要会分析实验数据,会从实验数据中找到有用的量.

练习册系列答案
相关题目
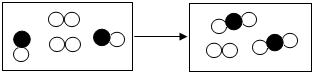
 ”和“
”和“ ”分别代表不同元素的原子,该反应可能是( )
”分别代表不同元素的原子,该反应可能是( )