题目内容
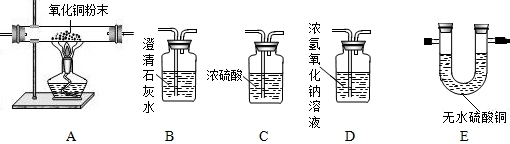
30、水蒸气通过炽热的焦炭得到的水煤气,其主要成分是CO和H2,还含有少量CO2和水蒸气,请用下列装置设计一个实验,以证明水煤气中含有CO和H2.

(1)连接上述所有装置的正确顺序是(用甲、乙、丙、丁、戊填入横线上):
水煤气→
(2)装置丁在连接时,气体必须由
(3)确认水煤气中含有H2的实验现象主要是
(4)确认水煤气中含有CO的实验现象主要是
(5)上述实验有何安全缺陷:

(1)连接上述所有装置的正确顺序是(用甲、乙、丙、丁、戊填入横线上):
水煤气→
丙
→戊
→甲
→乙
→丁
(2)装置丁在连接时,气体必须由
A
进入(用“A”或“B”填写)(3)确认水煤气中含有H2的实验现象主要是
甲中黑色物质变红乙中无水硫酸铜变蓝
.(4)确认水煤气中含有CO的实验现象主要是
甲中黑色物质变红丁中石灰水变浑浊
.(5)上述实验有何安全缺陷:
没有尾气的处理
.你认为应如何改进在B导管处点燃
.分析:(1)验证一氧化碳是利用一氧化碳与氧化铜反应既能还原氧化铜,又能生成二氧化碳,验证氢气是利用氢气与氧化铜反应既能还原氧化铜,又能生成水,所以要把原来的水和二氧化碳除掉;(2)根据除杂质的连接原则考虑;(3)考虑氢气还原氧化铜的现象和生成水的检验现象;(4)考虑一氧化碳还原氧化铜的现象和生成二氧化碳的检验现象;(5)由于一氧化碳还原氧化铜时尾气中会混有污染性气体,再考虑除去的方法.
解答:解:(1)要验证一氧化碳和氢气必须先除去原来的二氧化碳和水,要先通过氢氧化钠除去二氧化碳,再通过浓硫酸除去水,否则再通过氢氧化钠时,又会带上水,除完二氧化碳和水,再通过氧化铜,在验证生成物时要先验证有没有水,通过无水硫酸铜,看是否变蓝,变蓝说明有水生成,再通过石灰水看是否变浑浊,变浑浊说明有二氧化碳生成,即原气体中有一氧化碳;
(2)除杂质连接仪器的原则是:长进短出;
(3)由于氢气能还原氧化铜,使黑色粉末变成红色,并能生成水,能使白色的无水硫酸铜变成蓝色;
(4)由于一氧化碳能还原氧化铜,使黑色粉末变成红色,并能生成二氧化碳,使澄清石灰水变浑浊;
(5)由于一氧化碳还原氧化铜时尾气中会混有大量一氧化碳,而一氧化碳有毒,能污染空气,所以缺点是缺少尾气处理装置,应该将尾气点燃.
故答案为:(1)丙戊甲乙丁;(2)A;(3)甲中黑色物质变红乙中无水硫酸铜变蓝;(4)甲中黑色物质变红丁中石灰水变浑浊;(5)没有尾气的处理 在B导管处点燃.
(2)除杂质连接仪器的原则是:长进短出;
(3)由于氢气能还原氧化铜,使黑色粉末变成红色,并能生成水,能使白色的无水硫酸铜变成蓝色;
(4)由于一氧化碳能还原氧化铜,使黑色粉末变成红色,并能生成二氧化碳,使澄清石灰水变浑浊;
(5)由于一氧化碳还原氧化铜时尾气中会混有大量一氧化碳,而一氧化碳有毒,能污染空气,所以缺点是缺少尾气处理装置,应该将尾气点燃.
故答案为:(1)丙戊甲乙丁;(2)A;(3)甲中黑色物质变红乙中无水硫酸铜变蓝;(4)甲中黑色物质变红丁中石灰水变浑浊;(5)没有尾气的处理 在B导管处点燃.
点评:通过回答本题要知道除杂质时要把水放到最后除,如果验证水的存在时要把验证水的存在的无水硫酸铜放在最前面.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案
相关题目
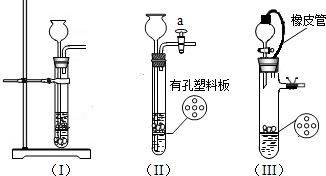
 (2006?眉山)(1)某化学活动小组对实验室制取气体的发生装置进行探究.下图是改进后的实验装置图:
(2006?眉山)(1)某化学活动小组对实验室制取气体的发生装置进行探究.下图是改进后的实验装置图: