题目内容
实验室中有一瓶失去标签的过氧化氢溶液,化学兴趣小组同学为了测定其溶质质量分数,取2g二氧化锰于锥形瓶中,然后慢慢滴入一定量的过氧化氢溶液,完全反应后产生1.6g氧气.锥形瓶中剩余物质的总质量是34.4g.计算这瓶过氧化氢溶液中溶质的质量分数.
解:依据质量守恒定律,向锥形瓶中滴入的过氧化氢溶液的质量为:34.4 g+1.6 g-2g=34 g.
设质量为x的过氧化氢分解能够产生1.6 g氧气.
2H2O2 2H2O+O2↑
2H2O+O2↑
68 32
x 1.6g

x=3.4 g
则这瓶双氧水的溶质质量分数为: =10%
=10%
答:这瓶过氧化氢溶液中溶质的质量分数为10%.
分析:依据质量守恒定律可得双氧水溶液的质量,而后依据氧气的质量求出反应的过过氧化氢质量,进而可以求出相关的答案;
点评:本题主要考查学生利用质量守恒定律、化学方程式和溶质质量分数公式进行计算的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.
设质量为x的过氧化氢分解能够产生1.6 g氧气.
2H2O2
 2H2O+O2↑
2H2O+O2↑68 32
x 1.6g

x=3.4 g
则这瓶双氧水的溶质质量分数为:
 =10%
=10%答:这瓶过氧化氢溶液中溶质的质量分数为10%.
分析:依据质量守恒定律可得双氧水溶液的质量,而后依据氧气的质量求出反应的过过氧化氢质量,进而可以求出相关的答案;
点评:本题主要考查学生利用质量守恒定律、化学方程式和溶质质量分数公式进行计算的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
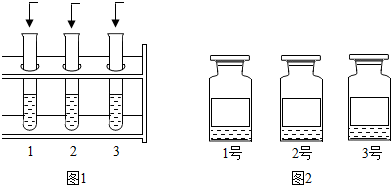

 老师在整理实验室时,发现一瓶失去部分标签的无色透明溶液.在一次实验课上,老师为了强调标签的重要性,特意拿出此瓶试剂让学生探究.
老师在整理实验室时,发现一瓶失去部分标签的无色透明溶液.在一次实验课上,老师为了强调标签的重要性,特意拿出此瓶试剂让学生探究.